心房利钠肽受体(NPR1),又称为NPRA或鸟苷酸环化酶A(GC-A),是心房钠尿肽NPPA/ANP和脑钠尿肽NPPB/BNP的受体,这些是强效的血管活性激素,在心血管稳态中发挥关键作用。NPR1结合配体后具有鸟苷酸环化酶活性。它在心衰,高血压心脏肥大等其他心血管疾病中发挥重要作用。
NPR1的表达
NPR1主要在脂肪细胞、分泌细胞、内皮细胞、成纤维细胞、II型肺泡细胞中表达。
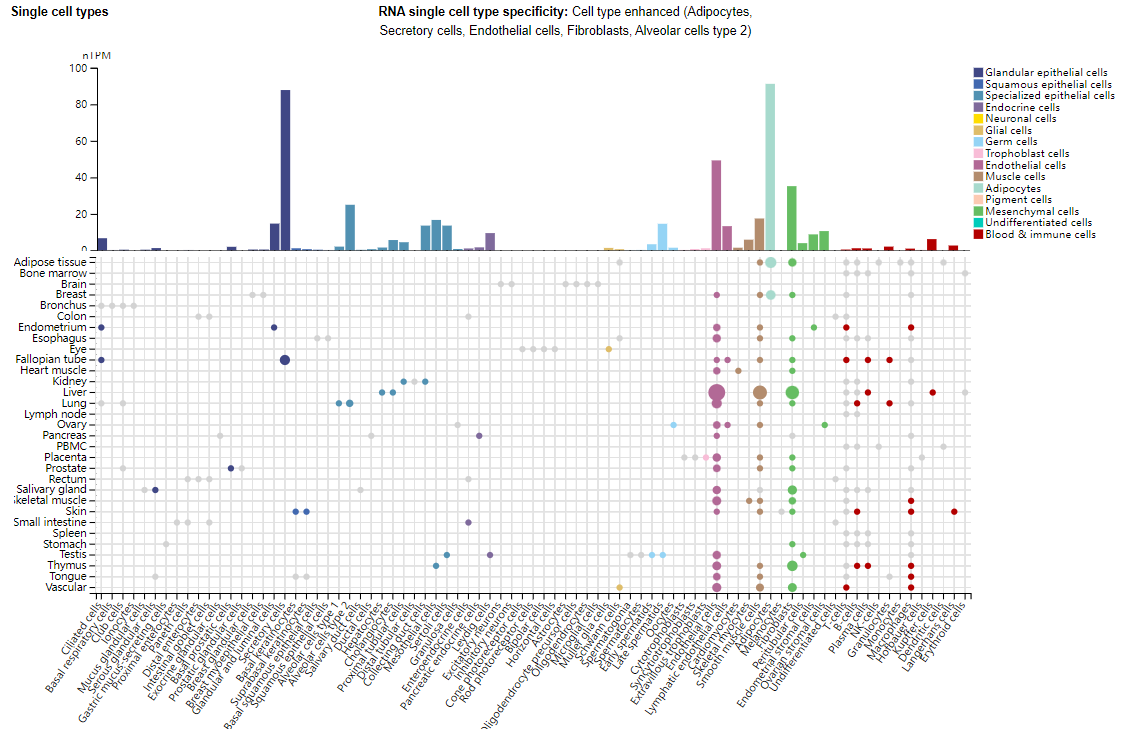
(数据来源 uniprot)
NPR1的结构
NPR1是型I膜蛋白,包含1个N端胞外区,跨膜区和C端胞质区。胞内区包括一个蛋白激酶样结构域和一个环化酶催化结构域,这些结构域参与下游信号转导;胞外区负责与ANP、BNP和CNP等利钠肽激素结合。NPRA在结构上倾向于自发二聚化,这对于其功能至关重要。

(数据来源 uniprot)
NPR1的信号通路和调控:
NPRA通过其细胞外结构域与配体ANP、BNP或CNP结合,导致受体发生构象变化。配体结合后,NPRA的同源二聚体结构域(蛋白激酶样结构域,protein-KHD)和鸟苷酸环化酶(GC)催化结构域被激活。激活的GC结构域催化ATP生成cGMP,cGMP作为第二信使在细胞内部扩散,激活cGMP依赖的蛋白激酶(PKG)、cGMP依赖的磷酸二酯酶(PDEs)和cGMP依赖的离子通道(如CNG通道)。cGMP可以介导血管舒张、心脏保护、抗增殖、抗炎、抗高血压和利尿等效应,这些效应有助于调节血压、心血管稳态和体液平衡。
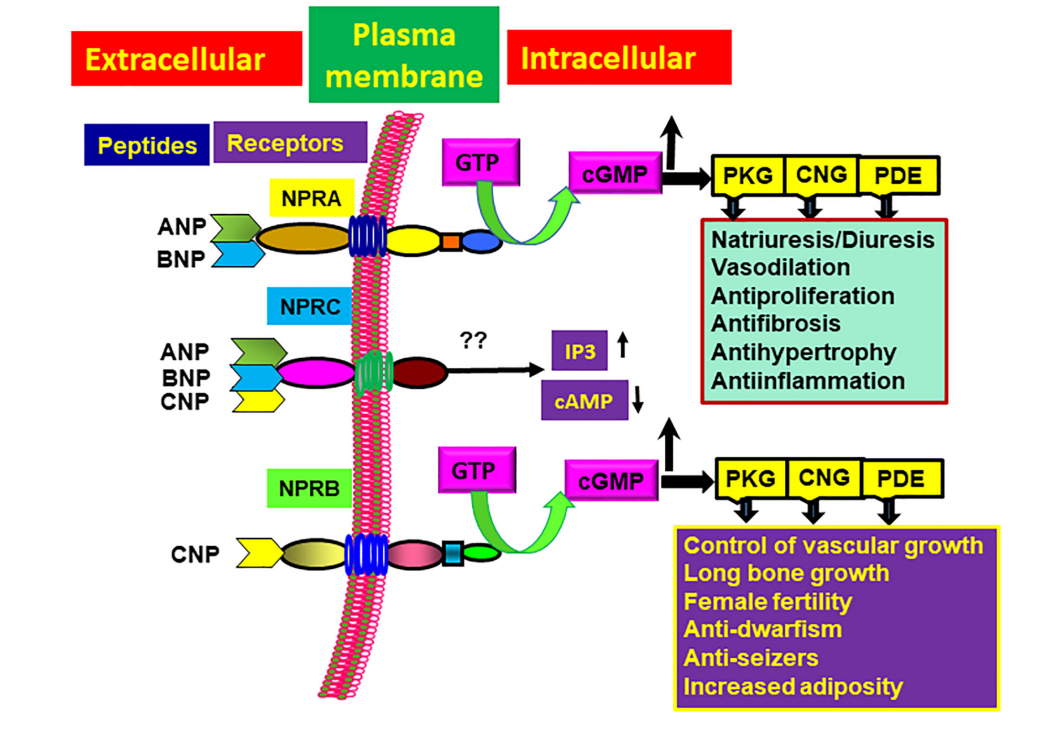
(数据来源 Pandey KN. Front Physiol. 2021)
NPR1与疾病
Npr1基因缺失会触发促炎途径的激活,导致心脏肥大、纤维化和重塑。ANP/NPRA信号通路的破坏导致NF-κB转录因子失衡激活,引发促炎细胞因子和基质蛋白的表达。激活的NF-κB进入细胞核,促进多种促炎细胞因子和细胞外基质蛋白的基因转录和表达,包括MMP-2和MMP-9。 NF-κB的过度激活促进中层增厚和血管周围纤维化,进而导致心脏肥大、纤维化、重塑和心力衰竭。ANP/NPRA信号的缺失同时抑制SERCA-2a,导致细胞内Ca2+水平升高,增加心脏的收缩活动,这也促进了心脏肥大和重塑。

(数据来源 Pandey KN. Front Physiol. 2021)
NPR1的靶向治疗
靶向NPR1的治疗策略主要包括开发NPRA激动剂,增强其与NPRA受体的结合亲和力和生物活性,从而更有效地激活NPRA。这可以提高细胞内cGMP水平,引发多种生理反应,如血管扩张、利尿、抗高血压等。
Imelciment(REGN5381)是由Regeneron Pharmaceuticals公司开发的一款靶向NPRA的单克隆抗体,是NPR1的变构激动剂,可诱导活性样受体构象。用于治疗慢性心力衰竭,射血分数降低的心力衰竭,心脏衰竭等疾病,目前处于临床2期研究阶段。REGN5381的Fab片段能够稳定NPR1的活性构象,防止其旋转回到非活性状态,从而需要较高的能量才能使Fab片段解离,这可能限制了不良药理学的潜力。REGN5381可能具有独特的安全性属性,即使在高剂量下,不良药理学的潜力也可能受到限制。

(数据来源 Dunn ME, et al. Nature. 2024)
REGN-7544是Regeneron Pharmaceuticals公司开发的另外一款靶向NPR1的单克隆抗体,用于治疗脓毒性休克,体位性心动过速综合征,处于临床2期研究阶段。

(数据来源 新药情报库)
我们收集整理一批NPR1相关抗体序列信息。文档可关注公众号“迈思生物”,号内回复“NPR1”下载。
