表皮生长因子受体(EGFR)是一种受体酪氨酸激酶,又称为HER1,ERBB。EGFR是一种细胞表面蛋白,可与表皮生长因子结合,从而诱导受体二聚化和酪氨酸自磷酸化,从而导致细胞增殖。EGFR突变或过表达一般会引发肿瘤,例如非小细胞肺癌(NSCLC)。
EGFR的分布
EGFR广泛分布于哺乳动物上皮细胞、成纤维细胞、胶质细胞、角质细胞等细胞表面,EGFR信号通路对细胞的生长、增殖和分化等生理过程发挥重要的作用。
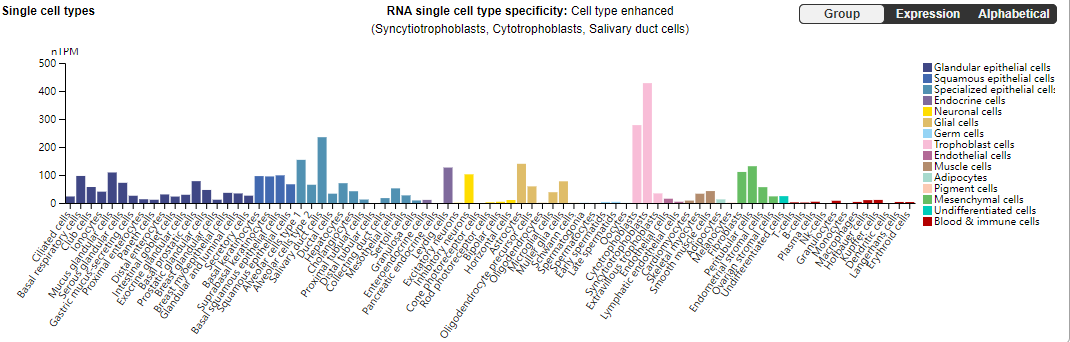
(数据来源 uniprot)
EGFR的结构
EGFR是一种跨膜糖蛋白,蛋白分子量大约为170KDa,EGFR由富含半胱氨酸的胞外配体结合结构域、疏水性跨膜结构域、胞质RTK结构域和C末端结构域组成。胞外区L1和L2是受体配体结合部位,CR1和CR2富含半胱氨酸残基,负责受体之间的二聚化。其胞内结构包含1个酪氨酸激酶域和具有多个自身磷酸化位点的羧基末端尾,小分子EGFR酪氨酸激酶抑制剂(TKI)的作用部位为胞内结构域。酪氨酸激酶结构域内的多个突变与EGFR-TKI的耐药性和敏感性相关。
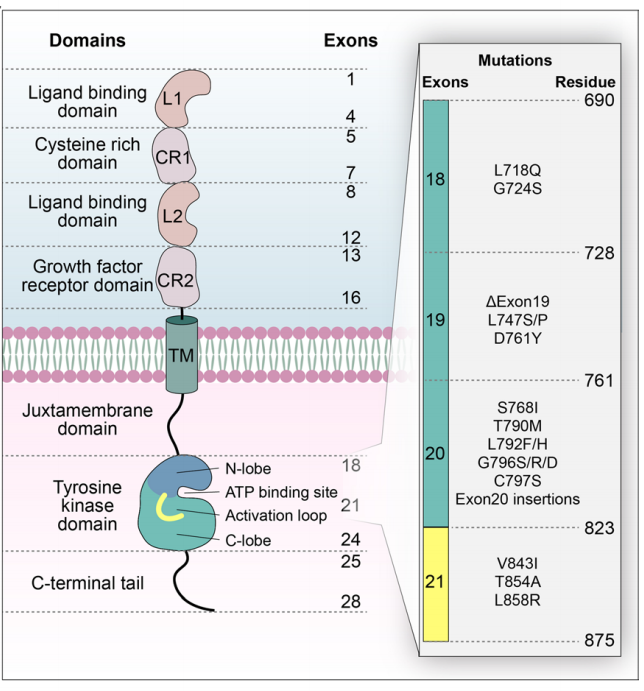
当EGFR处于活性状态时,在酪氨酸激酶结构域中,重要的催化残基D855位于ATP结合位点,稳定ATP负载复合物(DFG-in)和αC螺旋(αC-in)。在非活性状态下,EGFR形成Src样结构,包括闭合的A环、αC-out和DFG-in。
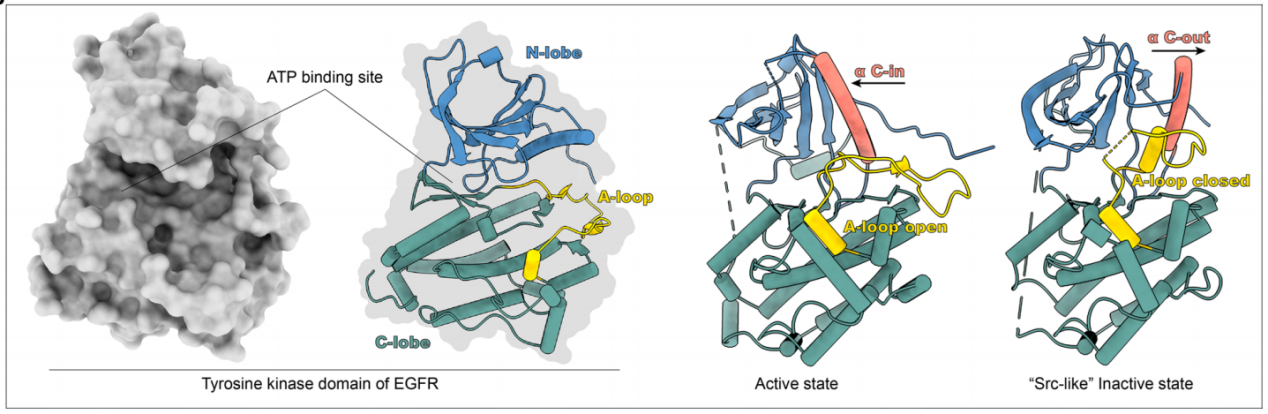
(数据来源 Shi K, et al. J Hematol Oncol. 2022)
EGFR的信号通路调控
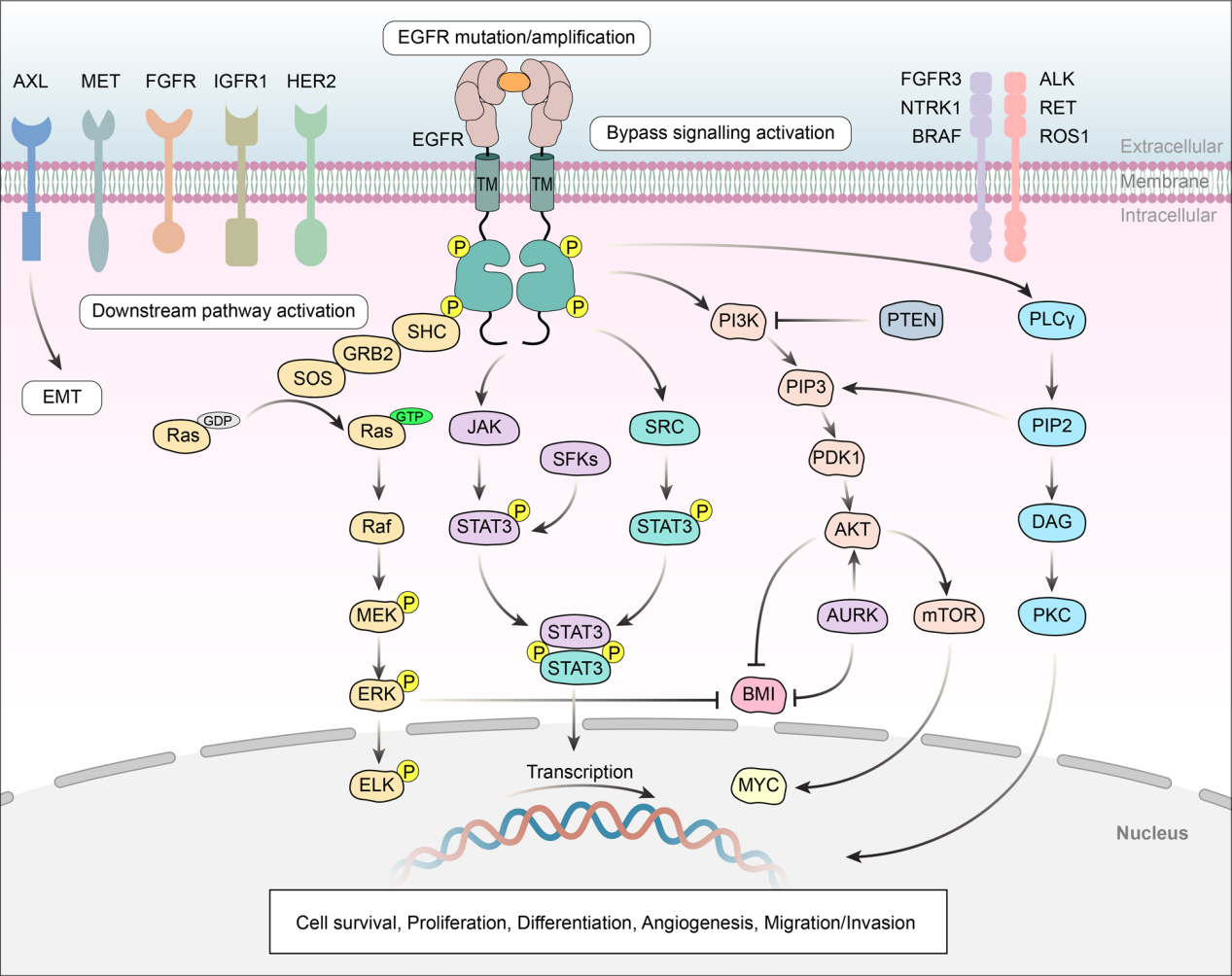
EGFR与特异性配体(如EGF,TGF-α)的结合导致受体的同型或异二聚化,从而导致细胞内激酶结构域的构象变化,从而导致受体的磷酸化和激活。信号轴RAS/RAF-MAPK和PI3K-AKT-mTOR依次激活各种下游信号通路,从而导致细胞增殖和生存的增强。

(数据来源 Shi K, et al. J Hematol Oncol. 2022)
EGFR药物的耐药机制
EGFR的耐药机制主要包括EGFR基因的二次突变(T790M突变,C797S突变),以及其他EGFR突变(如L718Q、L796S和L792H突变以及外显子20插入)、MET扩增、磷脂酰肌醇4,5-二磷酸3-激酶催化亚基α(PIK3CA)突变、HER2扩增、癌基因融合和细胞周期相关基因的改变。
受体酪氨酸激酶(receptor tyrosine kinases,RTKs)的扩增和突变均可诱导下游生存信号通路。此外,下游通路组分的直接过表达和/或突变可通过促进癌细胞生存而促进获得性耐药。
(数据来源 Shi K, et al. J Hematol Oncol. 2022)
EGFR的靶向治疗
目前针对EGFR的靶向治疗方式主要有两种方式:针对胞内域的小分子激酶抑制剂和针对EGFR胞外结构域或拮抗配体受体相互作用的单克隆抗体。但获得性耐药性阻碍了治疗结果的实现。抗ErbB方法的最新进展,例如双特异性抗体(BsAb),抗体偶联药物(ADC)旨在克服这种耐药性。
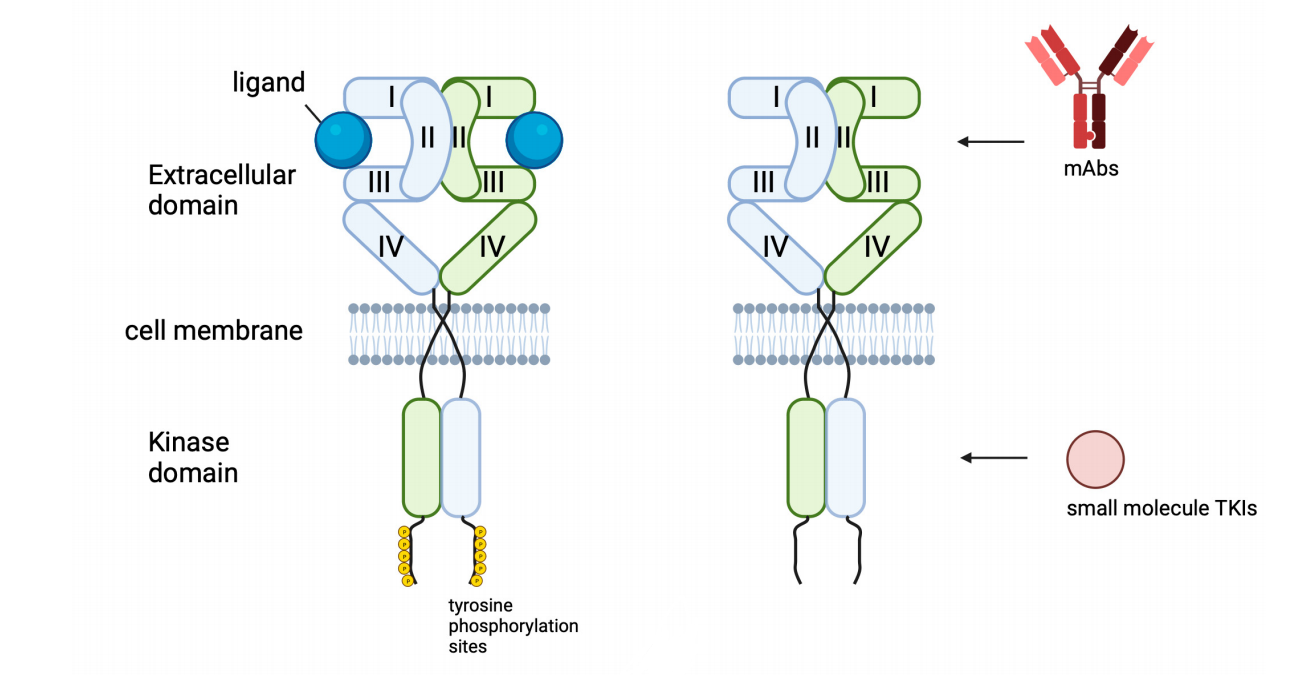
(数据来源 Shaban N, et al. Cells. 2023.)
EGFR的小分子激酶抑制剂
小分子药物通过竞争性抑制EGFR的ATP结合位点,阻止其激酶活性,从而抑制肿瘤细胞的增殖。根据开发时间和作用机制,可分为三代:
第一代TKIs:可逆性,非选择性抑制剂;如吉非替尼(Gefitinib)、埃克替尼(Erlotinib)等。
第二代TKIs:不可逆性,非选择性抑制剂;如阿法替尼(Afatinib)、达克替尼(Dacomitinib)等。
第三代TKIs(针对T790M突变):不可逆性,可选择性抑制剂;如奥希替尼(Osimertinib)、阿美替尼(Alectinib)等。

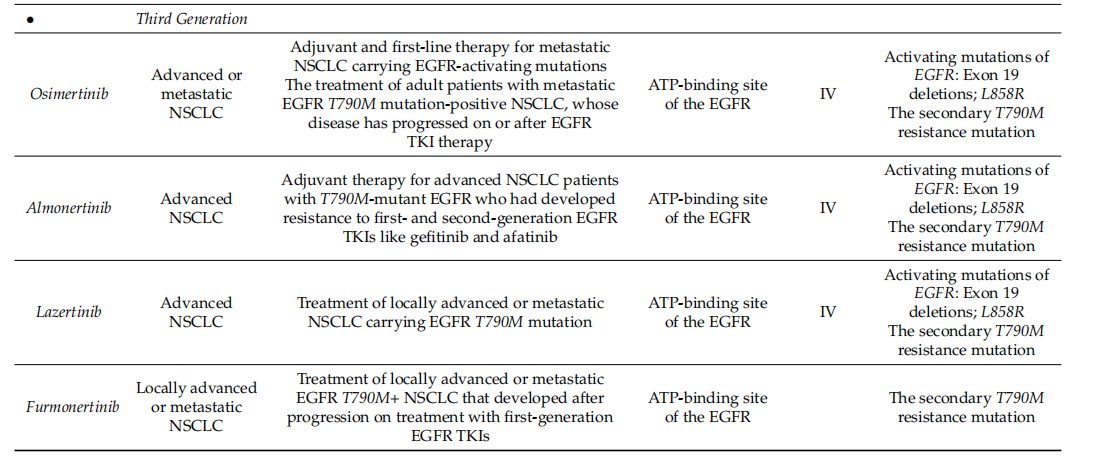
(数据来源 Shaban N, et al. Cells. 2023)
EGFR单克隆抗体
抗EGFR单克隆抗体通过结合EGFR蛋白的胞外域,抑制信号的传导,从而阻止细胞的繁殖和生存,最终导致细胞凋亡。已经获批上市的靶向EGFR的单抗有西妥昔单抗,恩立妥(西妥昔单抗β注射液),尼莫珠单抗,奈妥珠单抗,帕尼单抗。除此之外目前有许多抗体还在研究临床研究阶段。
恩立妥是一款于2024年6月获得中国国家药品监督管理局(NMPA)的批准上市的靶向EGFR的单克隆抗体,由抗肿瘤创新药公司先声再明与迈博药业合作研发。填补了中国结直肠癌EGFR靶向抗体药物近20年来仅有进口药物的空白。
Becotatug是一款由石药集团下属的津曼特生物开发的一款靶向EGRF的单克隆抗体,用于治疗EGFR阳性非鳞状非小细胞肺癌,EGFR突变的非小细胞肺癌,EGFR 20号外显子插入突变非小细胞肺癌等疾病,目前处于临床3期研究阶段。
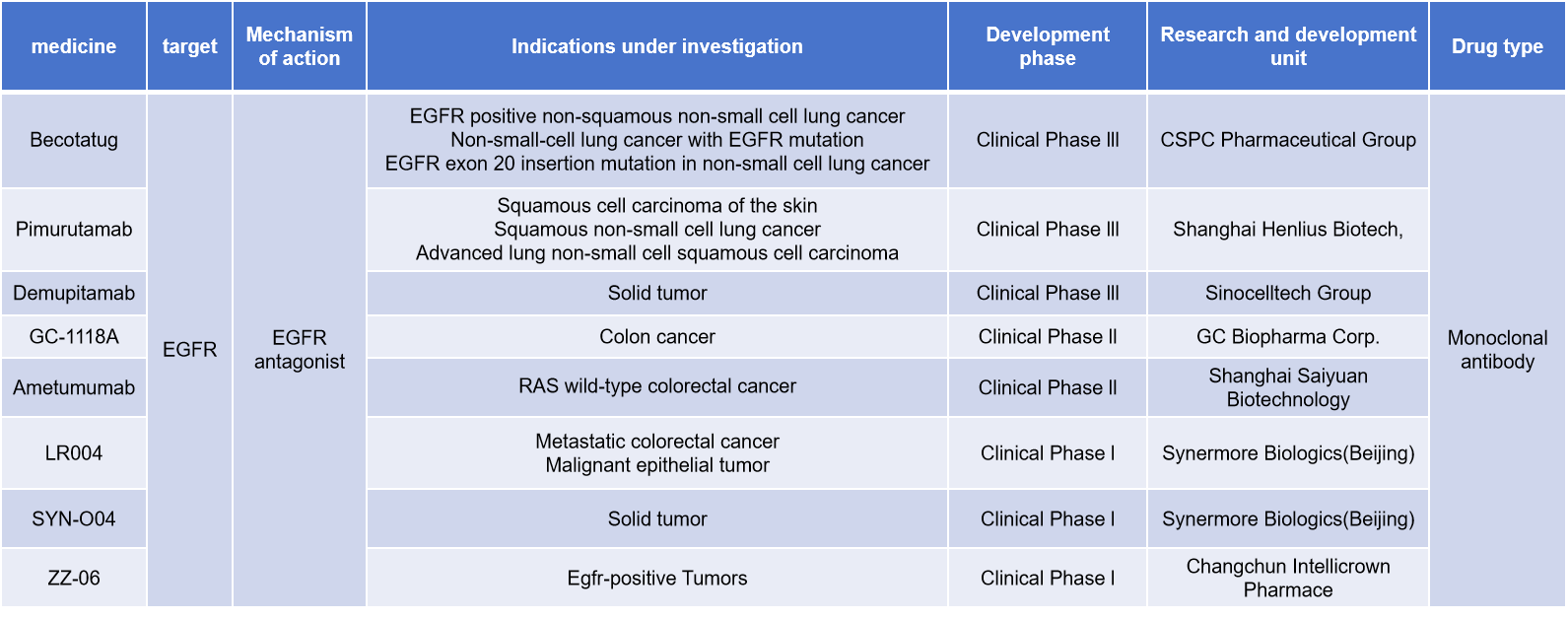
(数据来源 新药情报库)
EGFR/c-MET双靶点药物开发
EGFR与c-MET之间的相互作用在肿瘤生物学中扮演着复杂而重要的角色。由于c-MET的异常激活,c-MET的扩增或过表达可以绕过EGFR激活下游的信号通路,如PI3K/Akt和MAPK,从而促进肿瘤细胞的存活和增殖。针对EGFR和c-MET的双特异性抗体,可以同时阻断EGFR和c-MET介导的信号传导,从而抑制肿瘤细胞的生长和存活。这种双特异性抗体的开发为克服EGFR-TKI的耐药性提供了新的治疗策略。
Amivantamab是一款于2021年FDA批准上市的一款靶向EGFR和c-MET的双特异性抗体,由强生开发,它是全球首个获批用于治疗表皮生长因子受体20号外显子插入突变的局部晚期或转移性非小细胞肺癌成人患者的靶向治疗药物。研究发现将Amivantamab与Lazertinib联合治疗在治疗携带EGFR突变的晚期非小细胞肺癌(NSCLC)患者中显示出了显著的治疗效果,它延长了患者的中位PFS。

(数据来源 Felip E, et al. Ann Oncol. 2024)
目前还有许多EGFR/c-MET双靶点药物开发,其中包括4个双抗药物,1个三抗药物以及2个ADC药物。
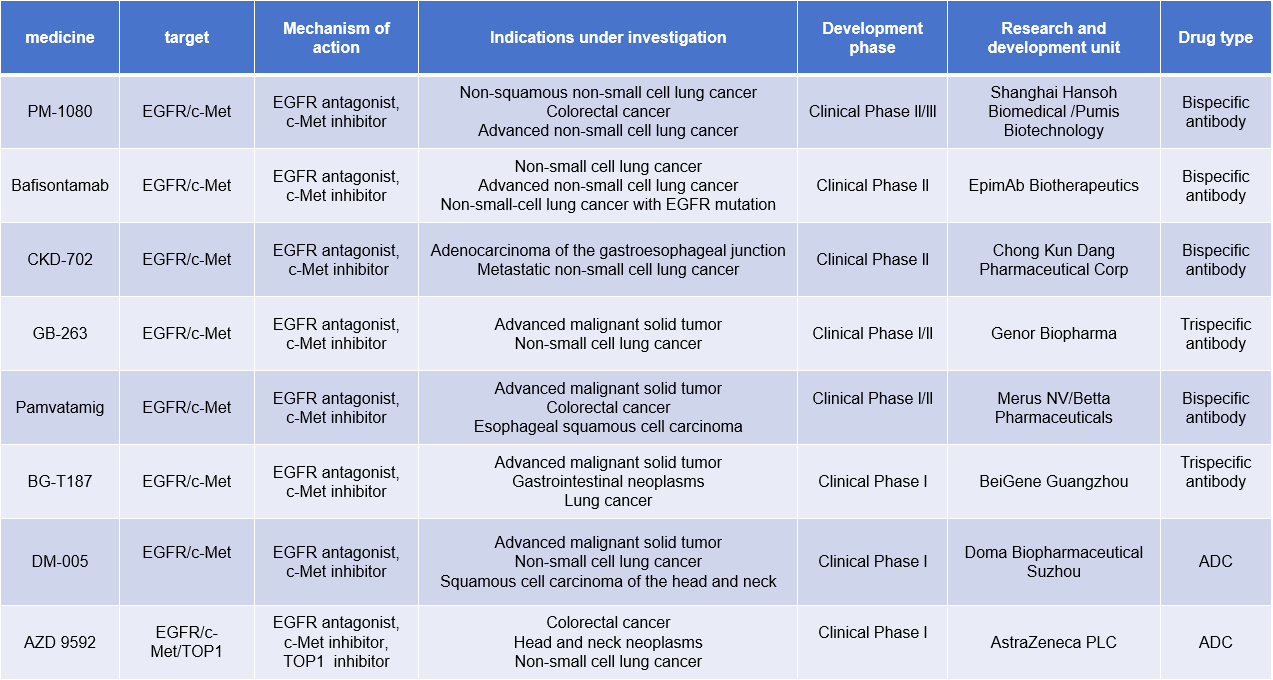
(数据来源 新药情报库)
PM-1080是由普米斯科技开发的一款靶向EGFR/c-MET的双特异性抗体,可通过特异性靶向肿瘤抗原EGFR和cMet来抑制肿瘤的生长和存活。用于治疗非鳞状非小细胞肺癌,结直肠癌,晚期非小细胞肺癌。
BG-T187由百济神州开发的一款靶向EGFR/c-MET的三特异性抗体,处于临床l期阶段,用于治疗晚期恶性实体瘤,胃肠道肿瘤,肺癌等疾病。
DM-005是一种全人EGFR/c-MET的双特异性抗体药物偶联物(ADC),由多玛医药开发,用于治疗晚期恶性实体瘤,非小细胞肺癌,头颈部鳞状细胞癌等疾病,处于临床l期研究阶段。DM-005的共轻链双抗结构是基于百奥赛图RenLite平台开发得到的,结构稳定,纯度高,DM-005使用的Linker-Payload为BLD1102(拓扑异构酶抑制剂)。DM-005双抗相较于其母本单抗表现出对双阳性肿瘤细胞系NCI-H1975更强的结合能力,内吞能力。
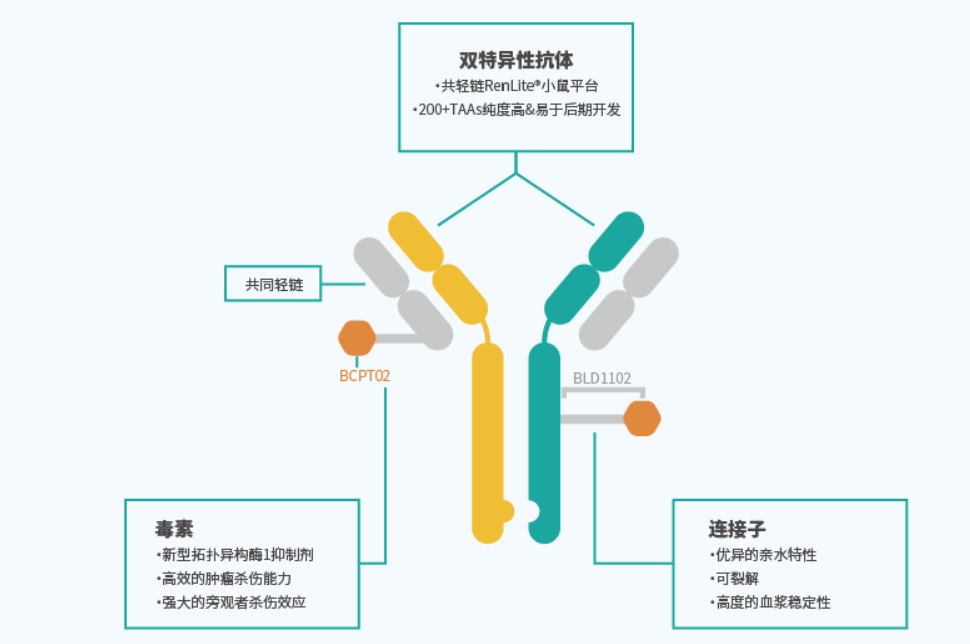
(数据来源 多玛医药官网)
我们收集整理一批EGFR相关抗体序列信息。文档可关注公众号“迈思生物”,号内回复“EGFR”下载。

