巨噬细胞迁移抑制因子(MIF)已被发现为T淋巴细胞诱导的抑制剂,可作为多效性促炎细胞因子。它参与了各种功能,包括白细胞募集,炎症,免疫反应,细胞增殖,肿瘤发生和糖皮质激素(GC)的反调节。
MIF的表达分布
MIF主要表达在T细胞,单核细胞、巨噬细胞、血液中的树突状细胞、B细胞、中性粒细胞、嗜酸性粒细胞、肥大细胞和嗜碱性粒细胞中,除此之外在腺上皮细胞,鳞状上皮细胞,特化上皮细胞,内分泌细胞也有表达。
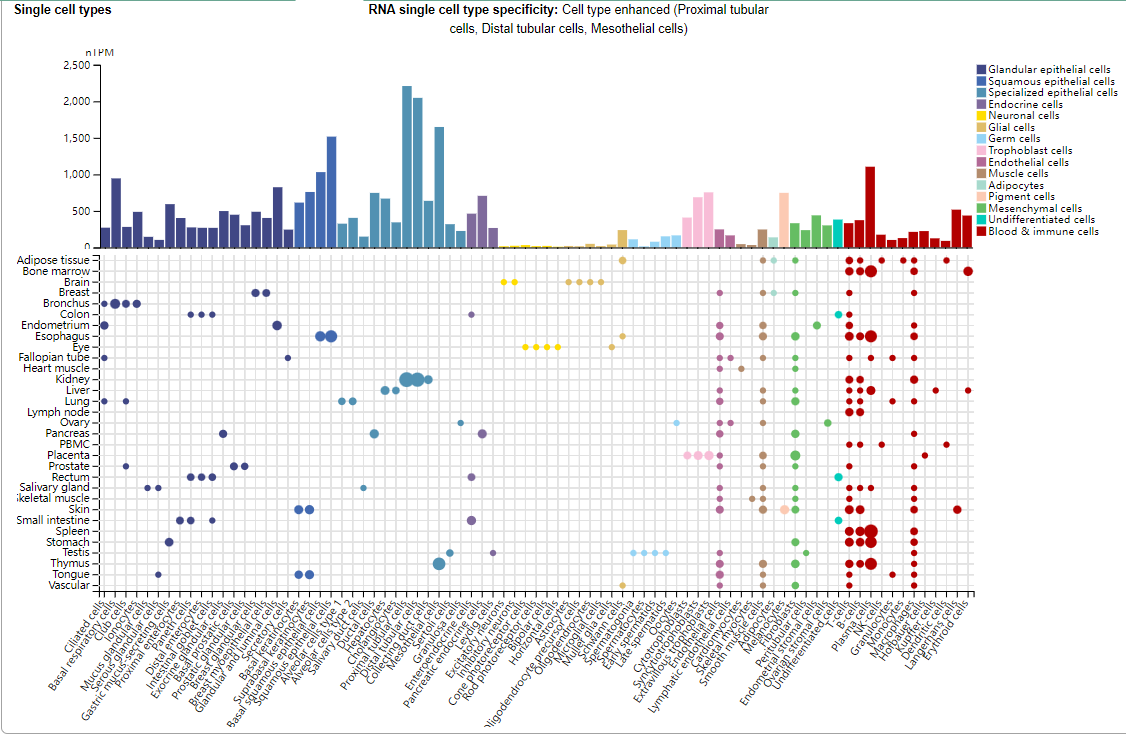
(数据来源 uniprot)
MIF的结构
MIF是一种由115个氨基酸组成的分泌蛋白,是一种高度保守的非糖基化蛋白,分子量为12.5 kDa。MIF是一个同源三聚体,而MIF超家族的另一个成员,D-DT/MIF2,是目前唯一一个与MIF具有相似功能谱的同源物。MIF是CD74,CXCR2,CXCR4和CXCR7的配体。
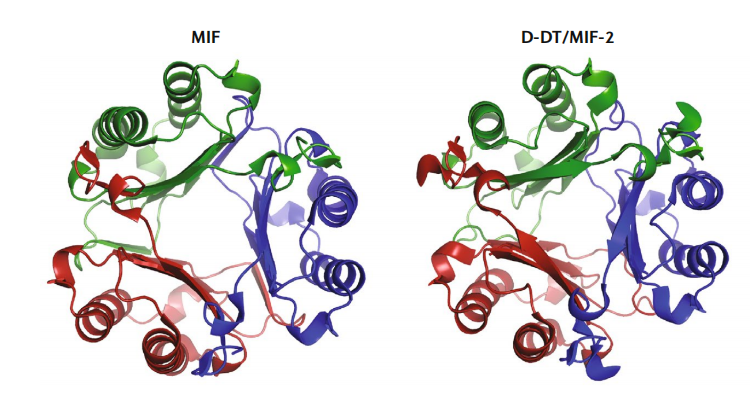
(数据来源 Kang I, et al. Nat Rev Rheumatol. 2019)
MIF的信号通路和调控
MIF以自分泌或旁分泌的方式发挥其生物活性,主要通过与细胞表面受体CD74相互作用,然后招募CD44形成受体复合物。此外,MIF还可以结合趋化受体,包括CXCR2、CXCR4和CXCR7。在受体结合后,MIF诱导下游信号通路的激活,包括丝裂原活化蛋白激酶(MAPK)、磷脂酰肌醇3/蛋白激酶B(PI3K/AKT)和NF-κB,这些信号通路通过诱导IL-6和TNF-α等促炎细胞因子的产生参与神经炎症,调节神经元存活和神经可塑性。此外,MIF可通过内吞作用直接进入细胞质,与JUN活化结构域结合蛋白1(JAB1)结合,调节AP-1活性和细胞增殖。MIF可以通过结合凋亡诱导因子(AIF)进一步转位到细胞核,导致DNA断裂和细胞死亡。
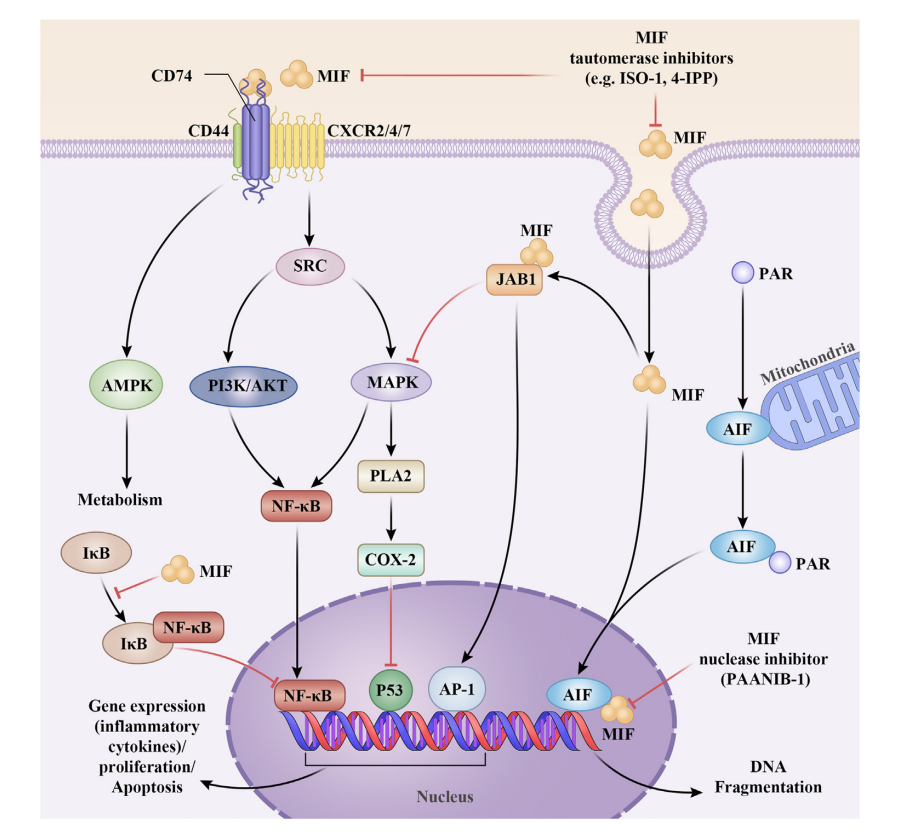
(数据来源 Zhang Y, et al. Fundam Res. 2023)
MIF在肿瘤中的作用
MIF在引发促肿瘤或抗肿瘤免疫反应中的功能是多种多样的,并且往往依赖于环境。一般来说,在早期肿瘤发生和生长过程中,MIF支持由早期浸润或常驻巨噬细胞和产生炎性IL-17的T淋巴细胞控制的促炎免疫表型,这些T淋巴细胞共同增加炎症,并可能导致细胞和组织损伤。随着肿瘤进展为体积更大、免疫抑制更强的晚期疾病,MIF表型开始更接近于伤口溶解活性,在这种情况下,MIF-肿瘤细胞衍生和免疫效应细胞衍生-在各种免疫细胞类型中启动促肿瘤免疫逃避和新生血管过程。
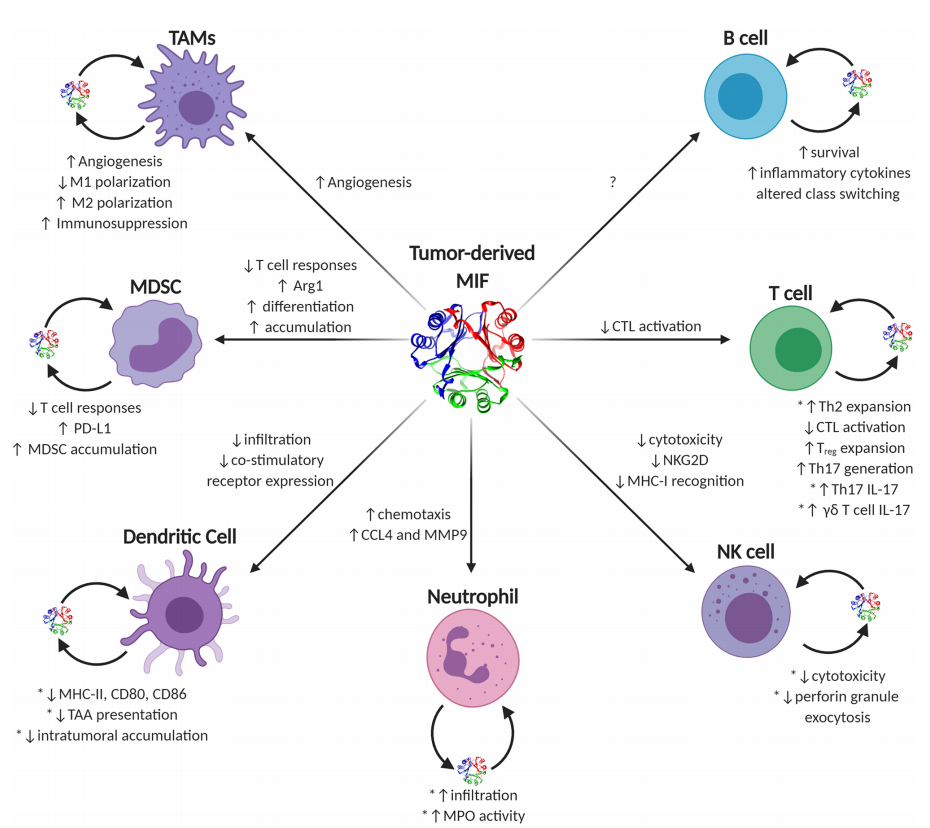
(数据来源 Noe JT, Mitchell RA. Front Immunol. 2020)
MIF的靶向治疗
MIF在炎症性和自身免疫性疾病发病机制中发挥重要作用,MIF已成为一种有吸引力的新型疾病治疗靶点。神经内分泌轴是指导炎症反应的重要调控系统,MIF是垂体前叶细胞在受到刺激后的主要分泌蛋白,这使得研究者们更加关注MIF功能的评估和MIF靶向治疗。目前基于MIF的治疗策略是肿瘤学研究的前沿领域。MIF靶向治疗主要是小分子抑制剂,目前也有许多靶向MIF的抗体在临床开发中。
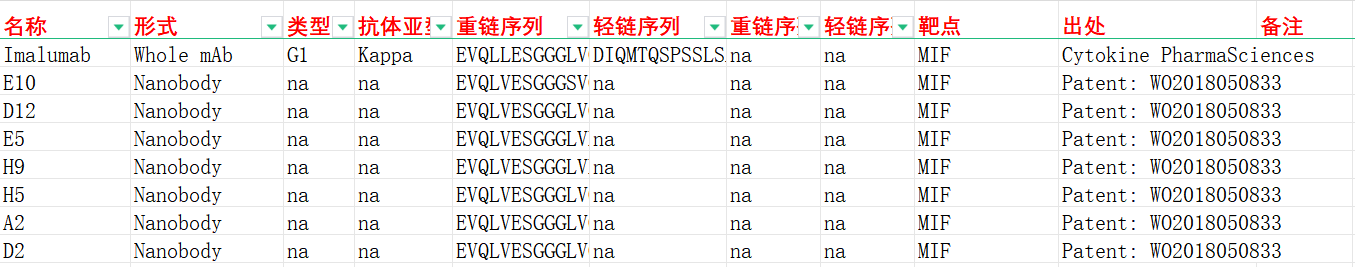
Imalumab是一种靶向MIF的单克隆抗体,用于治疗结直肠癌和腹水。一项1期研究(NCT01765790)评估了Imalumab对实体瘤的安全性、药代动力学、耐受性和抗肿瘤活性。Imalumab的最大耐受剂量为每2周37.5 mg/kg(静脉给药),剂量限制性毒性为实体瘤患者的过敏性肺泡炎。Imalumab还被评估用于恶性腹水的卵巢癌患者(NCT02540356)以及与5-FU/亚叶酸钙或Panitumumab联合用于转移性结直肠癌(mCRC)患者(NCT02448810)。然而,这两项研究均因设计不足和整体获益-风险评估而提前终止。
我们收集整理一批MIF相关抗体序列信息。文档可关注公众号“迈思生物”,号内回复“MIF”下载。