NY-ESO-1是一种自身免疫性癌抗原,也称为CTA1B(CTAG1B),由主要组织相容性复合体I类分子呈现在细胞表面,在生殖细胞和各种癌症中表现出受限表达。NY-ESO-1既是肿瘤相关抗原,又是其自身佐剂,它具有作为损失相关分子模式的潜在功能。它引发强烈的体液免疫反应,特定抗体频率与疾病进展显着相关。这些特性使NY-ESO-1成为开发有效和特异性免疫疗法的有吸引力的候选药物,特别是针对晚期疾病。

2024年9月14日研究人员在Clinical and translational medicine上发表了一篇名为“NY-ESO-1 antigen: A promising frontier in cancer immunotherapy”的文章,该文章描述了NY-ESO-1作为免疫原性肿瘤抗原的情况,并探索了针对NY-ESO-1的各种策略,包括使用肽、蛋白质、DNA、mRNA、细菌载体、病毒载体、树突状细胞和人工佐剂载体细胞进行癌症疫苗接种,同时考虑了每种策略的优缺点。并介绍了一种创新的技术,将下一代NY-ESO-1 T细胞产品和与淋巴结靶向疫苗的结合,以应对挑战并提高治疗效果。

NY-ESO-1的表达分布
在睾丸、卵巢和多种癌症中表达。在子宫肌层中检测到。在人类胎儿睾丸中从18周开始表达直至出生。在成人睾丸中,在精原细胞和初级精母细胞中强烈表达,但在减数分裂后细胞或睾丸体细胞中不表达。
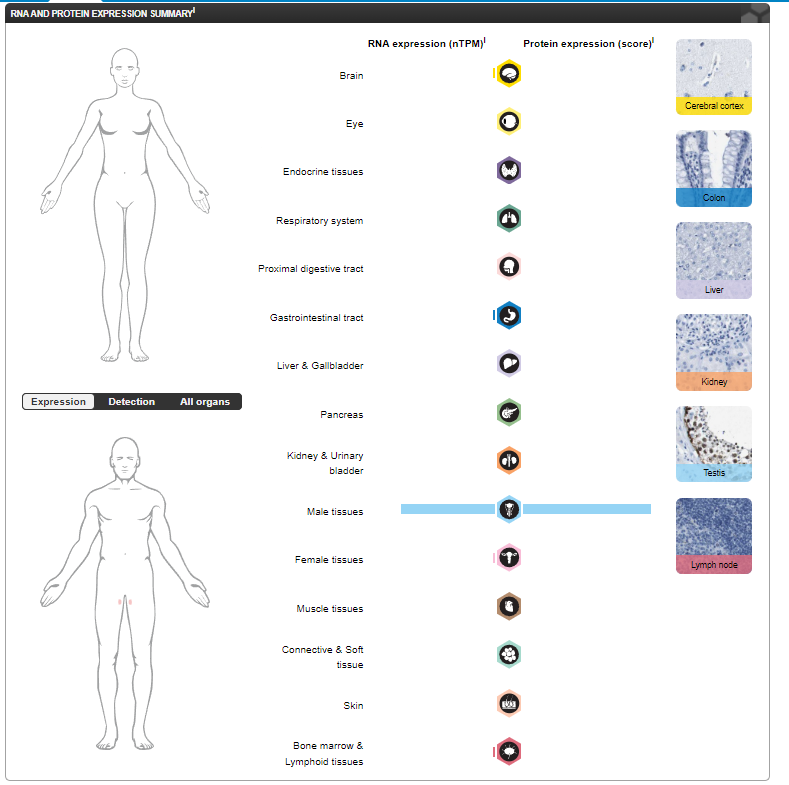
(数据来源 uniprot)
NY-ESO-1的结构
NY-ESO-1由位于X染色体Xq28区域的CTGAG1B基因编码,它是一种分子量为18kDa的180个氨基酸的蛋白质。它在其富含甘氨酸的N端区域和以及带有Pcc-1结构域的疏水C端区域,保守的Pcc-1结构域的存在表明其可能参与调节细胞周期进程和生长。

(数据来源 AlphaFold)
NY-ESO-1作为免疫原性抗原肿瘤
NY-ESO-1具有高度免疫原性。它在约50%的NY-ESO-1表达肿瘤患者中引发了自发抗体反应,并且已经证明NY-ESO-1的特异性抗体滴度与疾病的进展和肿瘤分期而变化。
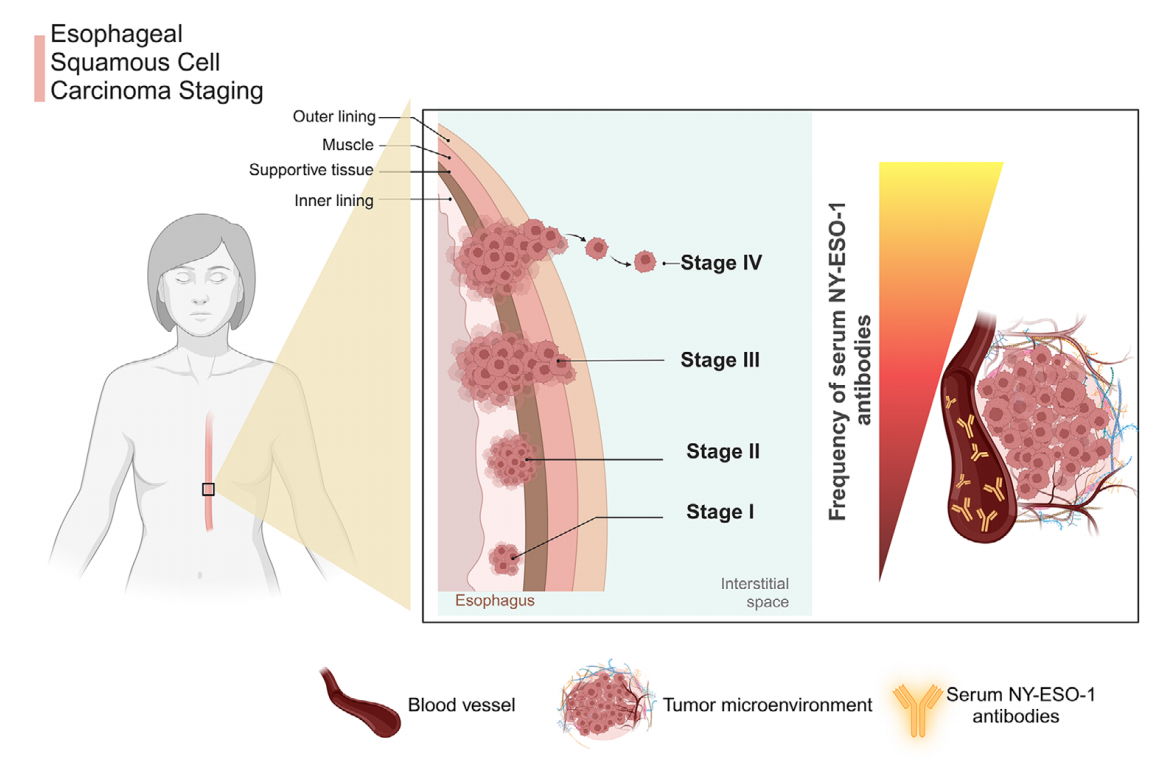
血清NY‐ESO-1抗体(s‐NY‐ESO-1-Abs)是食管癌的独特生物标志物,与其他类型的癌症相比,食管癌患者的s-NY-ESO-1-Abs阳性率明显较高。
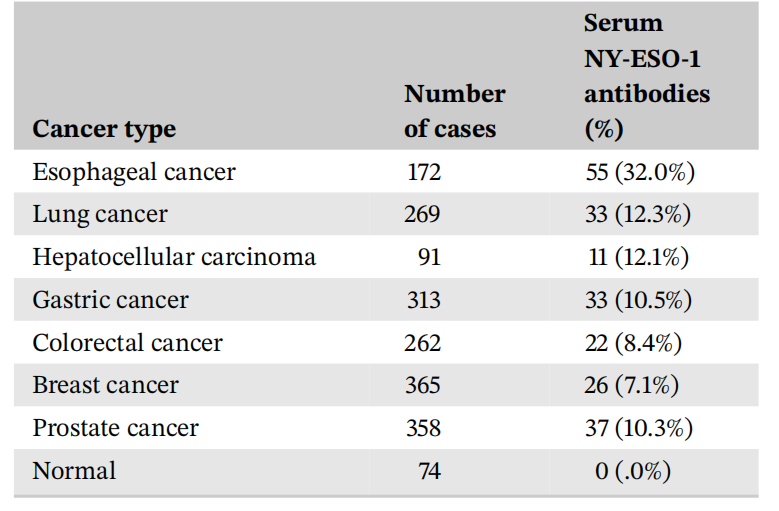
NY-ESO-1在肿瘤微环境中的免疫机制
在肿瘤微环境中,从坏死癌细胞释放的NY-ESO-1与未成熟树突状细胞(DC)表面的补体C1q受体和Toll样受体4(TLR4)结合。NY-ESO-1与CRT-TLR4的结合会诱导吞噬作用,导致DC成熟。随后,成熟的DC迁移到淋巴结并呈递NY-ESO-1肽,引发一系列免疫事件,导致对各种癌症类型的自发免疫。

NY-ESO-1癌症疫苗
NY‐ESO-1癌症疫苗具有多种模式,包括肽、蛋白质、DNA、mRNA、病毒载体、细菌载体、人工佐剂载体细胞(aAVC)和基于DC的疫苗。
肽和蛋白质类疫苗:在肿瘤微环境中,抗原呈递细胞(APC)处理并呈递与MHC分子结合的肽,CD8+CTL对肽-MHC 复合物的识别触发了它们的激活,从而导致肿瘤特异性CTL的扩增,CTL能够靶向和消除表达TAA的癌细胞。

研究发现NY‐ESO-1蛋白或肽类疫苗的临床试验都强调重组肽/蛋白与佐剂同时给药,这种方法旨在增强化学稳定性和免疫刺激特性,从而促进产生强大的免疫反应。一项临床I期研究(NCT00616941)发现将poly-ICLC加入乳剂中促进了NY-ESO-1特异性抗体的产生,增强了CD4+T细胞反应并维持了CD8+T细胞反应。
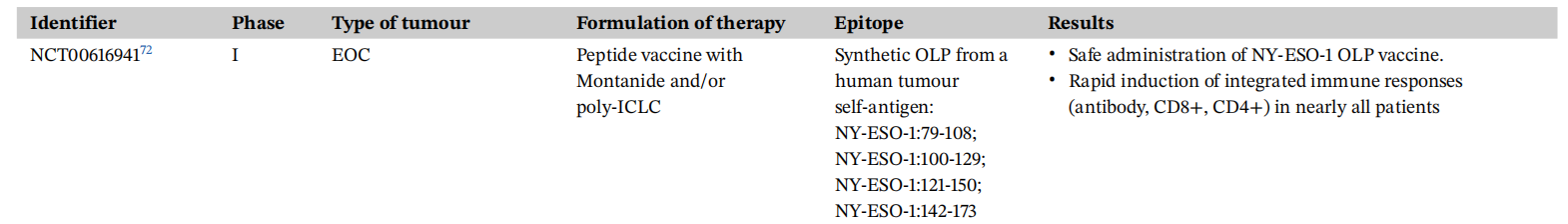
许多临床试验将NY-ESO-1疫苗接种与其他方式相结合,以增强治疗效果。例如,在一项II期研究中(NCT02129075),CDX-301预处理可增加树突状细胞数量,并增强由CDX-1401疫苗接种引起的对NY-ESO-1的反应,该方案可作为预防高风险黑色素瘤患者疾病复发的预防性疫苗。
当疫苗与PD-1单克隆抗体结合时,肿瘤抑制效果良好,暗示了未来治疗的潜在方向。目前已启动多项临床试验,以探索涉及肽NY-ESO-1癌症疫苗的联合疗法,包括检查点抑制剂(例如NCT01176474、NCT02737787、NCT01176461)、去甲基化剂(例如NCT02750995、NCT03358719、NCT01673217)和吲哚胺2,3‐双加氧酶抑制剂(NCT02166905)。
核酸疫苗:核酸疫苗具有强大的佐剂特性,可以分为DNA疫苗和RNA疫苗,采用全长肿瘤抗原的基因序列,允许呈现多个表位并引发强大的T细胞反应。在RNA疫苗的开发中,利用噬菌体RNA聚合酶,从编码抗原的DNA模板体外合成RNA。
DNA疫苗:DNA疫苗利用质粒作为载体来运输编码肿瘤抗原的基因,从而刺激或增强抗原特异性免疫反应。NY-ESO-1 DNA疫苗已被证明可在癌症患者中引发强烈的CD4+和CD8+T细胞反应。但是可能存在调节性T细胞机制,会削弱疫苗的功效。科学家将16个NY-ESO-1表位(涵盖80%以上的HLA表型)整合到互补决定区(CDR)中,以开发人类IgG DNA(SCIB2)。SCIB2疫苗接种通过高亲和力Fc受体靶向体内树突状细胞,导致肿瘤显著消退,并且比肽疫苗接种诱导更频繁、亲和力更强的强效T细胞反应。当与Treg耗竭、细胞毒性T淋巴细胞抗原4(CTLA-4)阻断或 PD-1阻断相结合时,SCIB2疫苗接种在已患肿瘤的个体中表现出更高的长期生存率。
DNA疫苗稳定,简单,性价比高,但是可能会存在质粒DNA整合到宿主基因组中的潜在风险。
mRNA疫苗:以RNA为基础的癌症疫苗使用脂质体和鱼精蛋白-mRNA纳米颗粒作为递送系统,在促进其递送到细胞的同时封装和保护mRNA免受降解。在一项针对晚期黑色素瘤患者的I期试验(NCT02410733),编码NY-ESO-1等四种TAA的FixVac(BNT111)RNA疫苗,单独使用或与检查点抑制剂联合使用均可诱导持久的客观反应、强大的T细胞免疫力和显著的抗肿瘤作用。

微生物载体疫苗:微生物载体疫苗主要通过MHC I类和II类途径诱导抗原呈递,它主要分为细菌疫苗和病毒疫苗。这些疫苗利用宿主的先天免疫监视机制,引导免疫系统瞄准和消灭肿瘤。
细菌疫苗:细菌充当内在免疫刺激剂,携带与病原体相关的分子模式,可触发免疫细胞上的模式识别受体(如 TLR)。这种参与会引发强烈的先天免疫反应,从而有效地破坏免疫耐受性。一种利用鼠伤寒沙门氏菌的疫苗被设计成通过III型蛋白分泌系统将NY-ESO-1抗原直接递送到APC中。这种疫苗在小鼠中表现出有效性,并且能够在具有预先存在的NY-ESO-1免疫力的癌症患者中引发NY-ESO-1特异性CD8+和CD4+T细胞反应。鼠伤寒沙门氏菌-NY-ESO-1疫苗促使没有固有NY-ESO-1免疫力的黑色素瘤患者产生CD4+T辅助细胞1(Th1)细胞。
病毒疫苗:病毒疫苗利用转基因病毒作为载体,靶向癌细胞,促进细胞内抗原的表达,引发强烈的CTL反应,最终消灭受病毒感染的细胞。腺病毒和痘苗病毒是被广泛研究的载体之一,它们具有显著的免疫刺激能力,尤其是激活CTL,而不需要使用佐剂。在一项涉及患有各种晚期实体瘤的患者的临床试验中,研究人员使用重组牛痘-NY-ESO-1(rV-NY-ESO-1)作为初免,随后使用重组鸡痘-NY-ESO-1(rF-NY-ESO-1)作为加强。这种顺序给药旨在增强免疫反应,而不会引发宿主中和免疫。
vCP2292(ALVAC(2)-NY-ESO-1(M)-TRICOM)疫苗的临床前研究表明,将编码各种共刺激分子(TRICOM、B7-1、ICAM-1和淋巴细胞功能抗原3(LFA-3))的转基因与NY-ESO-1转基因一起整合到重组ALVAC(2)痘病毒中,可增强NY-ESO-1特异性T细胞免疫反应。
基于树突状细胞的疫苗:树突状细胞要么用肽脉冲,要么用肽转导,既作为疫苗接种的佐剂,又作为疫苗接种的递送系统。研究发现DC疫苗耐受性良好,在近一半患者中诱导出功能性NY-ESO-1特异性T细胞。目前,装载了多种肽(包括NY-ESO-1)的最先进的DC疫苗正在临床试验的不同阶段进行评估(NCT03970746)。
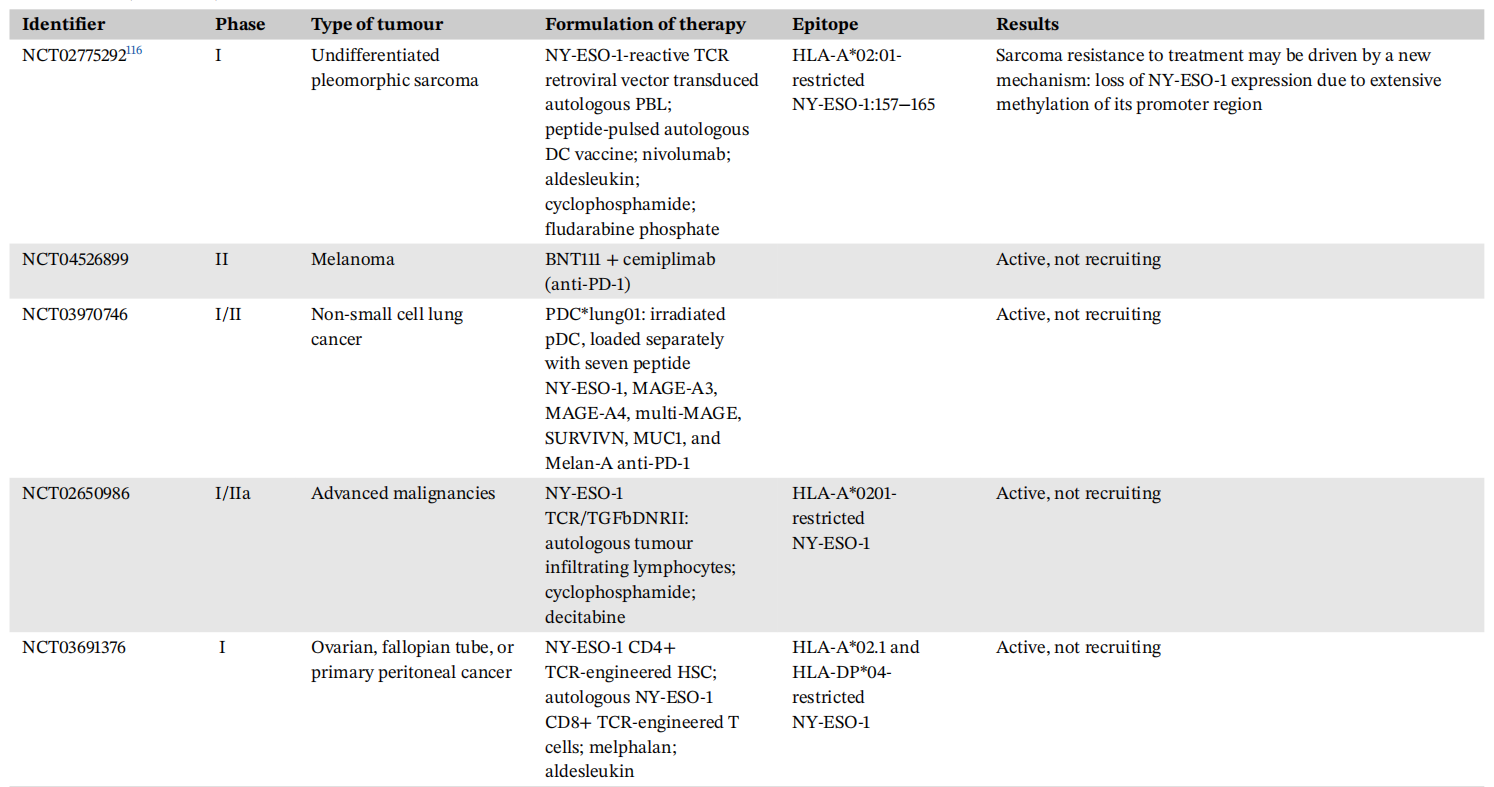
人工佐剂载体细胞疫苗:Fujii、Shin-Ichiro等人开发了一种针对NY-ESO-1的aAVC(aAVC-NY-ESO-1)。这种创新疫苗有效刺激了针对NY-ESO-1的特异性CTL反应,同时还激活了iNKT和自然杀伤(NK)细胞。它促进了DC的成熟,并促进了NY-ESO-1抗原的交叉呈递,从而在临床前小鼠模型中产生了显著的抗肿瘤作用。
全细胞疫苗:全细胞疫苗通过使免疫系统接触癌细胞表达的全部抗原,这种广泛的接触有可能激活多种免疫细胞,包括T细胞、B细胞和NK细胞,从而增强对癌症的免疫反应。在一项临床前研究中,肾癌细胞经过基因改造后可表达NY-ESO-1抗原,然后注射到患有NY-ESO-1阴性肾肿瘤的小鼠体内。这种治疗方法可显著缩小肿瘤体积,并增强树突状细胞和T细胞之间的相互作用。这些结果表明,即使在不自然表达NY-ESO-1的肿瘤中,NY-ESO-1也可以作为佐剂发挥作用,有效训练先天免疫细胞和T细胞识别和靶向具有更高免疫原性的肿瘤表位。
过继性T细胞治疗:在一项研究(NCT01352286)中,NY-ESO-1 SPEAR T细胞在80%的多发性骨髓瘤患者中表现出积极的临床反应。这些细胞表现出细胞毒性活性和持久性,导致中位PFS为1.5年。后续研究证实了持续的疗效,包括迁移到骨髓和在部分患者中持续的肿瘤靶向作用。两项正在进行的I期临床试验(NCT01946373、NCT01697527)分别在探索过继T细胞转移与DC疫苗接种在黑色素瘤和晚期恶性肿瘤中的结合。

NY-ESO-1的创新疗法
通过将TCR T细胞疗法与淋巴结靶向疫苗相结合,可以建立有利于抗原扩散的淋巴环境。这种组合已被证明有望改善对TCR T细胞单一疗法有抗性的小鼠实体瘤的持久反应,并增强免疫系统对原始治疗重点以外的肿瘤特异性靶点的识别,从而促进长期保护。一项I期临床试验(JMA-IIA00346)将NY-ESO-1特异性TCR工程化T细胞疗法与淋巴结靶向纳米颗粒肽疫苗相结合。
其他研究人员正在研究将NK细胞作为T细胞的替代品,其中包括对脐带血来源的NK细胞进行工程改造,使其表达NY-ESO-1 TCR/IL-15细胞受体,结合CD3和TCR信号复合物,以特异性地靶向NY-ESO-1抗原。这种方法在治疗实体瘤方面的疗效目前正在I/II期临床试验中进行评估(NCT06066359)

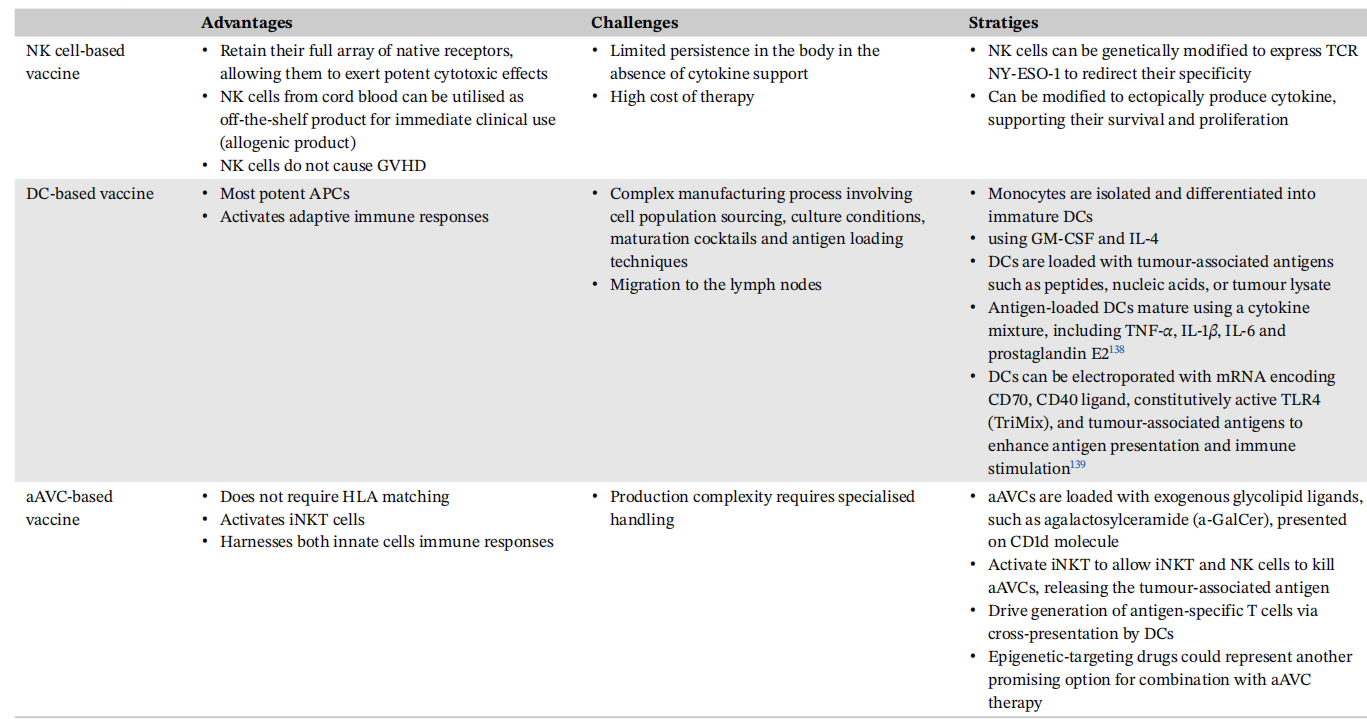
NY-ESO-1的癌症免疫疗法比较
NY-ESO-1癌症免疫疗法多种多样,他们有着不同的机制和优势以及不足。例如,使用DC疫苗作为直接佐剂可能会进一步增强治疗潜力,但是制造工艺复杂;NY-ESO-1特异性TCR工程细胞疫苗可有效杀死肿瘤细胞,但是受HLA相容性限制,对遗传T细胞进行工程改造需要数周的生产时间。努力克服当前挑战和探索创新策略对于充分实现NY-ESO-1的治疗潜力至关重要。

我们收集整理一批NY-ESO-1相关抗体序列信息。文档可关注公众号“迈思生物”,号内回复“ NY-ESO-1”下载。
