背景
糖基化是生物体内蛋白质修饰的一种关键方式,通过影响蛋白质折叠,运输和定位,在调节各种生物学功能中发挥重要作用。糖基化模式的变化是癌症的重要特征,与癌症相关过程中的一系列病理活动有关,并作为重要的生物标志物为癌症诊断和治疗提供新的靶点。乳腺癌的人表皮生长因子受体2(HER2)、肝癌的甲胎蛋白(AFP)、结肠癌的癌胚抗原(CEA)和前列腺癌的前列腺特异性抗原(PSA)等糖蛋白都是已获准用于临床的肿瘤生物标志物。
2024年9月21日,湖南省人民医院肿瘤科研究人员在Cancer communications(London,England)上发表了一篇名为“Altered glycosylation in cancer: molecular functions and therapeutic potential”的文章,该文章介绍了糖基化结构的多样性和新发现的糖基化底物—糖基化RNA(glycoRNA)。本文主要从肿瘤转移、免疫逃避、代谢重编程、异常铁死亡反应和细胞衰老等方面阐述糖基化在癌症中的作用。此外,还总结了蛋白质糖基化在癌症诊断、治疗和多药耐药性方面的临床应用,展望了蛋白质糖基化的临床应用前景。

糖基化的结构和生物学功能
蛋白质糖基化是糖链通过糖基转移酶和二磷酸核苷酸酶附着在蛋白质上的某些氨基酸上。糖基化有助于蛋白质的正确折叠,糖基化在生物学中也发挥重要作用,包括受体相互作用和促进细胞间信号转导。根据糖基化位点的不同,可以分为N-糖基化,O-糖基化,C-糖基化和糖基磷脂酰肌醇。
N-糖基化:O-糖基化是指N-聚糖中的N-乙酰葡萄糖胺(GlcNAc)与天冬酰胺(Asn)氨基的氮原子通过β1-糖苷键共价连接。这种变化通常发生在保守的糖基化模式Asn-X-Ser/Thr中的特定Asn位点,其中“X”代表脯氨酸以外的任何氨基酸。N连接糖基化是一个受到严格调控的过程,涉及一系列协调的翻译后事件,导致细胞表面、分泌和循环蛋白的修饰和改变。N连接多糖合成与蛋白质折叠、内质网稳态以及溶酶体和自噬中的许多作用密切相关。缺乏N-糖基化的蛋白质无法被内质网中的钙联蛋白(CNX)和钙网蛋白(CRT)正确识别,从而导致低糖基化蛋白质错误折叠及其降解。
O-糖基化:当多糖与多肽丝氨酸或苏氨酸残基的氧原子的羟基结合时,会发生O-糖基化。与丝氨酸和苏氨酸氨基酸连接的主要糖是N-乙酰葡萄糖胺(GlcNAc)和N-乙酰半乳糖胺(GalNAc)。O-GlcNAc糖基化影响蛋白质结构的构象和稳定性,介导蛋白质-蛋白质相互作用及其生物受体的分子识别。
C-糖基化:C-糖基化是一种相对罕见的糖基化修饰,由α-D-甘露吡喃糖基通过CC糖苷键与色氨酸(Trp)残基连接而成。Trp-XX-Trp/Cys/Pro是C-糖基化位点的氨基酸序列,其中X代表任何氨基酸。C-糖蛋白约占分泌或嵌入细胞膜的蛋白质的20%。C-甘露糖基化过程对于蛋白质的正确折叠、分泌和稳定性至关重要。
糖基磷脂酰肌醇:糖基磷脂酰肌醇(GPI)是一种结构复杂的糖脂化合物,GPIT复合物是一种跨膜酶,可促进GPI与内质网内的蛋白质结合,从而帮助GPI锚定蛋白(GPI-AP)成熟。GPI-AP蛋白参与其他生物过程,如生物合成、运输、细胞膜分布和信号转导、细胞粘附和抗原呈递。
GlycoRNA:它是指在细胞表面的RNA上发生的糖基化,糖基化RNA可以作为细胞膜Siglec受体的直接配体。Siglec受体在免疫调节中的重要作用,糖基化RNA在各种生理和病理过程中发挥着至关重要的作用,如宿主免疫反应、肿瘤逃避免疫系统和自身免疫性疾病。glycoRNA可以促进免疫系统中的细胞间通讯。细胞表面的glycoRNA对中性粒细胞募集至关重要。P-选择素(SELP)促进中性粒细胞和内皮细胞之间的通讯,从而实现对它们的识别。

糖基化在癌细胞中的作用
糖基化修饰蛋白参与细胞内多种生物过程。异常糖基化与许多疾病过程密切相关,当癌症中的糖基化未得到适当调节时,会导致信号传导中断、癌细胞扩散以及逃避免疫系统检测。
糖基化与肿瘤转移:糖基化过程的破坏,特别是糖链结构、糖基转移酶活性和糖基化底物表达的破坏,会影响与肿瘤扩散相关的事件,例如癌症干细胞(CSC)的特征、上皮间质转化(EMT)。它也会影响一系列致癌信号通路,从而引发肿瘤的侵袭和转移。例如,B3GNT5糖基化与基底样乳腺癌中的癌症干细胞特性有关。SLC35A2通过调节糖基化来增加细胞粘附能力,从而促进HCC转移。

糖基化与肿瘤免疫逃逸:随着癌症的进展,肿瘤细胞会适应免疫系统的选择性压力,慢慢地发展出逃避检测的方法。肿瘤细胞的糖基化在规避有效的免疫应答中起关键作用。例如,GALNT7修饰前列腺癌细胞中与免疫信号通路相关的O-糖基化。在乳腺癌细胞中,ST3GAL1对CD55的O联唾液修饰有助于乳腺癌细胞免疫逃避。FUT8介导的异常B7H3糖基化抑制TNBC细胞中的免疫反应。B4GALT1介导PD-L1蛋白的N连接糖基化,从而防止PD-L1在转录后水平降解。TGF-β1介导的PD-L1糖基化通过c-Jun/STT3A信号通路促进免疫逃避。TMUB1通过招募STT3A增强PD-L1N-糖基化和稳定性,从而促进PD-L1成熟和肿瘤免疫逃避。O-GlcNAcylation阻碍PD-L1的溶酶体降解,促进肿瘤免疫逃避。

糖基化与肿瘤代谢重编程:蛋白质的糖基化在癌细胞的代谢重编程中至关重要,可协调代谢途径以产生促进肿瘤发展的必要代谢物。糖基化增加PGK1的代谢酶活性,并诱导PGK1易位至线粒体以抑制TCA循环,从而增强癌细胞中的Warburg效应。PIGT通过调节GLUT1糖基化增强膀胱癌细胞的糖酵解。O-GlcNAcylation调节MDH1的代谢活性,促进胰腺癌中的谷氨酰胺代谢。SCAPN-糖基化促进SCAP/SREBP易位至高尔基体,进而激活SREBP1,通过SREBP依赖性脂质调节肿瘤中的脂质代谢。

糖基化与铁死亡:糖基化与癌症中铁死亡相互作用,调节肿瘤发展。铁蛋白重链的去糖基化增强了其与铁蛋白吞噬细胞受体NCOA4的相互作用,导致不稳定铁在线粒体中积聚,从而导致铁死亡。抑制4F2hc的N-糖基化通过抑制谷氨酸-胱氨酸反向转运系统Xc-的活性来增强PDAC细胞的铁死亡敏感性。USP8通过稳定OGT来抑制肝细胞癌中的铁死亡敏感性,OGT会促进SLC7A11的O-GlcNAc酰化。葡萄糖诱导的ZEB1O-GlcNA酰化激活脂肪生成相关基因FASN和FADS2的转录活性,导致间充质胰腺癌细胞中脂质过氧化依赖性铁死亡。

糖基化与细胞衰老:衰老细胞逃避免疫监视可能通过DNA损伤和氧化应激等机制促进肿瘤的发生和进展。细胞渗透性抑制剂NGI-1以寡糖基转移酶为目标,阻断细胞表面定位和EGFR糖蛋白信号传导,促进细胞衰老。KRAS突变肺癌细胞中O-GlcNAc酰化水平升高会抑制KrasG12D OIS并加速肺部肿瘤发生。

糖基化在癌症中的治疗潜力
基于糖基化的肿瘤生物标志物:许多糖蛋白,如肝癌的AFP,结肠癌的CEA,和前列腺癌的前列腺特异性抗原(PSA),已被临床批准作为肿瘤生物标志物。高度糖基化的HCG是人类滋养细胞早期侵袭的标志。糖基转移酶和糖苷酶的异常表达在糖链和糖蛋白的紊乱中起着关键作用。因此,这些酶可以被认为是癌症的潜在的可行性生物标志物。例如,胃癌中的POFUT1,黑色素瘤中的GCNT2都可被作为肿瘤生物标志物。

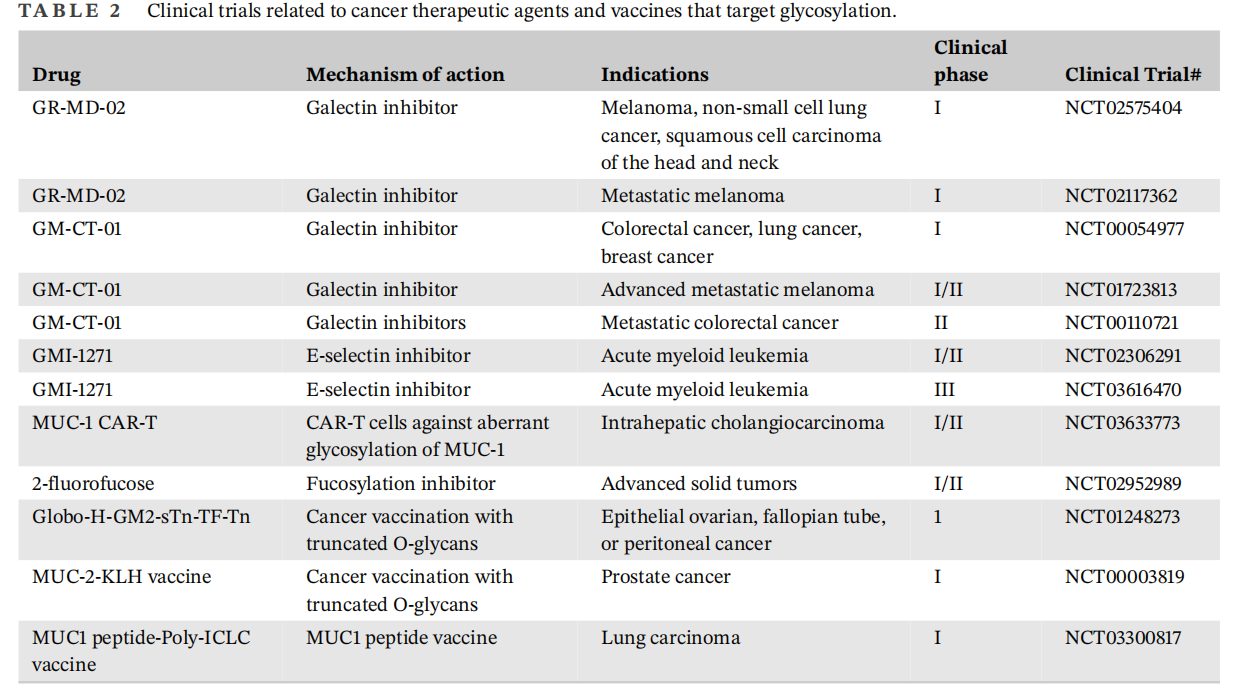
糖基化与肿瘤治疗:研究发现糖基化在多种药物获得性耐药的出现至关重要。Tunicamycin是一种有效的糖基化抑制剂,通过糖基化抑制作用,在各种类型的肿瘤中显示出显著的抗肿瘤效果。靶向抑制肿瘤糖基化是克服胃癌患者化疗耐药的可行性方法。靶向MUC1的糖基化是改善胃癌耐药的一种有前景的策略。干扰肿瘤细胞的N-糖基化可显著提高CAR-T细胞治疗实体瘤的疗效。ALG3已被证明可以通过修饰TGFBR2的糖基化来增加乳腺癌患者的放射抗性,并促进肿瘤干细胞的生长。目前有许多靶向糖基化的药物和疫苗正在进行治疗癌症的临床试验。
总结
糖基化影响蛋白质的折叠,在生物学功能和肿瘤免疫治疗中发挥着重要作用,异常糖基化的研究为癌症的进展提供了新的视角。研究异常糖基化的机制和识别糖蛋白生物标志物将有助于癌症治疗的进步,为早期发现和治疗提供科学指导。未来糖组学和糖基化研究的发展可能会显著改善当前的癌症治疗格局。