丰富的纤维化间质是大多数实体肿瘤的典型特征,间质激活促进肿瘤发生、治疗耐药和癌细胞转移播散。因此,靶向肿瘤间质结合标准治疗成为近年来很有前景的治疗策略。富含亮氨酸的重复序列蛋白(LRRC15)参与细胞-细胞和细胞-基质相互作用。由于其在间充质来源的肿瘤(如肉瘤、胶质母细胞瘤和黑色素瘤)以及乳腺癌、头颈部、肺和胰腺肿瘤微环境中的癌症相关成纤维细胞中过表达,因此成为一个有前景的抗癌靶点。使用特异性抗体-药物偶联物(ADC)有效靶向LRRC15有可能改善间充质来源或间质结缔组织增生的LRRC15阳性(LRRC15+)癌症患者的预后。此外,LRRC15的表达可以作为一个预测生物标志物,用于癌症患者的临床前评估,以支持个性化的临床结局。

(数据来源 Ray U, et al. Cancer Res. 2022)
LRRC15的表达分布
LRRC15主要在淋巴内皮细胞中表达,LRRC15的正常组织表达定位于构成先天免疫屏障的区域,如胎盘、皮肤、伤口内活化的成纤维细胞和淋巴组织(如脾脏)。LRRC15可能在固有免疫中发挥一定作用。


(数据来源 uniprot)
LRRC15的结构
LRRC15是位于3号染色体3q29的跨膜蛋白,属于LRR超家族,LRRC15包含15个LRR序列。LRR基序在不同长度的重复延伸中的结构安排为几种蛋白质-蛋白质相互作用创造了适应性框架。这些LRR序列形成了一个马蹄形的结构,其中凹面由平行的β-折叠组成,凸面则由不同的二级结构(如α-螺旋)组成。N末端由一个保守的富含亮氨酸的11-残基序列组成。具有LRR结构域的蛋白通常参与多种蛋白质相互作用,包括细胞黏附、受体-配体结合和目标识别。

(数据来源 Alphafold)
LRRC15在癌症中的作用
LRRC15在许多实体瘤基质内的癌症相关成纤维细胞(CAF)中高表达,并在胶质母细胞瘤、肉瘤和黑色素瘤等间充质肿瘤中直接表达。LRRC15通过与纤维连接蛋白和β1整合素的相互作用促进转移,导致黏着斑激酶信号的激活。LRRC15最近被证明通过调节Wnt/β-catenin信号通路促进三阴性乳腺癌(TNBC)肿瘤的迁移和侵袭。TNBC细胞系CAFs中LRRC15的高表达与胞质和胞核β-catenin的增加相关,β-catenin驱动癌细胞迁移和侵袭。在机制上,LRRC15的表达降低了Axin1的表达,Axin1是促进β-catenin降解的破坏复合体的蛋白成员,导致β-catenin水平升高。表达CAFs的LRRC15促进了TNBC细胞系中基质金属蛋白酶(MMP)的表达,这进一步介导了迁移和侵袭。然而,LRRC15对MMP表达的影响可能是背景依赖的,因为星形胶质细胞中LRRC15的表达与MMP的过表达无关。
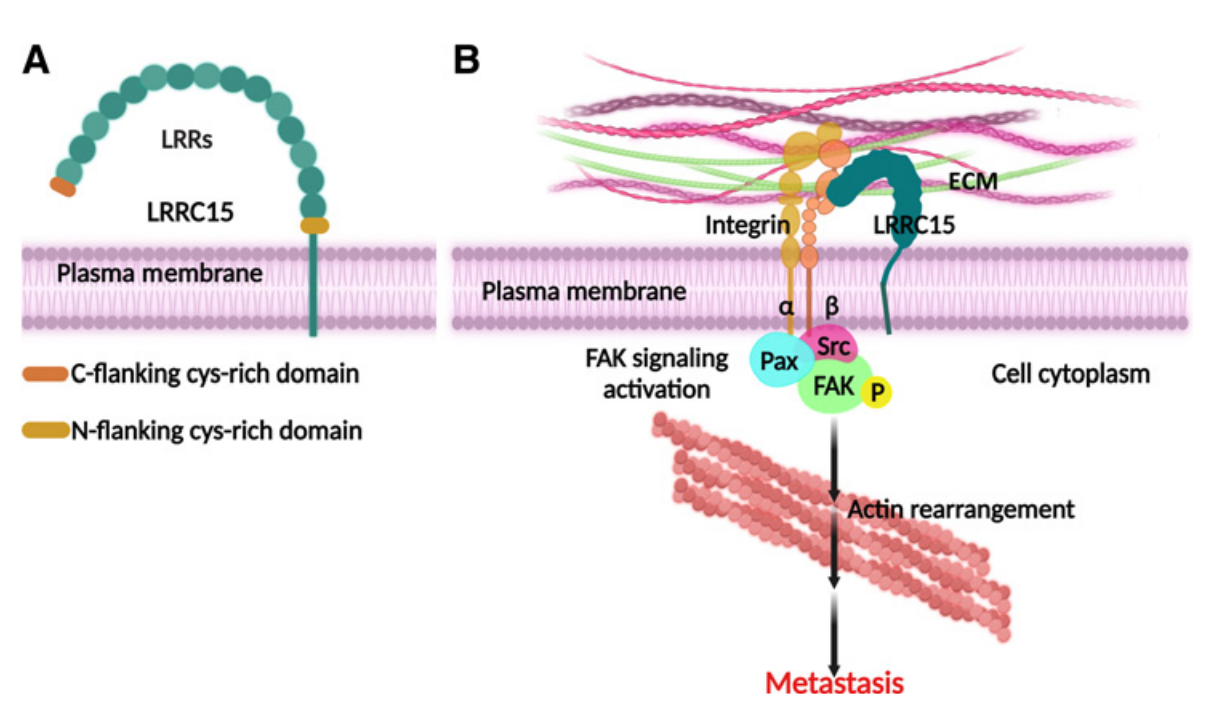
(数据来源 Ray U, et al. Cancer Res. 2022)
LRRC15的靶向治疗
目前开发针对LRRC15的靶向治疗方式是抗体药物偶联物(ADC),ABBV-085(Samrotamab vedotin)是一种抗LRRC15人源化IgG1抗体,由AbbVie开发。ABBV-085已完成肉瘤和其他晚期实体瘤的I期首次人体安全性研究(NCT02565758)。进行了一项非随机、多中心、I 期、开放标签、剂量递增研究,以确定ABBV-085的药代动力学和安全性,并评估建议的II期剂量,作为单一疗法或与标准治疗联合治疗用于晚期实体瘤患者,包括肉瘤、头颈部鳞状细胞癌和乳腺癌。据报道ABBV-085疗法通常耐受性良好,安全性可控,并且在难治性肉瘤适应症中显示出令人鼓舞的抗肿瘤活性迹象。虽然目前ABBV-085没有最新的进展,但是ABBV-085在临床上的初步结果,已证明了新靶点LRRC15作为实体瘤治疗的可行性。
ZL-6201是由再鼎医药与宜联生物合作开发的一款靶向LRRC15的ADC用于治疗实体瘤,目前在临床前研究。ZL-6201已在临床前研究中展现出令人鼓舞的数据,预计将于2025年提交IND(新药临床研究申请)。
我们收集整理一批LRRC15相关抗体序列信息。文档可关注公众号“迈思生物”,号内回复“LRRC15”下载。

