生长抑素受体(SSTR2)是一种G蛋白偶联受体(GPCR)超家族,产生发生在中枢神经系统,特别是下丘脑,以及消化系统和胰腺。它对激素分泌,细胞周期,细胞凋亡和血管生成具有多种作用。生长抑素受体SSTR2表达是分化良好的神经内分泌肿瘤(NET)的标志,它是NET的潜在治疗靶点。
SSTR2的表达
SSTR2广泛分布在人多个组织器官中,在大脑中广泛表达,在胰腺的α细胞和β细胞中均有表达,在胰腺中的表达水平高于其他生长抑素受体。肾脏,空肠、结肠和肝脏中也有表达。在发育中的神经系统中,在皮质中表达,早期位于前板,后期在生发区的外部富集。在小脑中,在妊娠第19周时在外部颗粒层的深部表达。这种模式持续到出生,但在成年后消失。
在肿瘤组织中,SSTR2在神经内分泌瘤中高表达,还表达在脑膜瘤、乳腺癌、前列腺癌、结直肠癌。
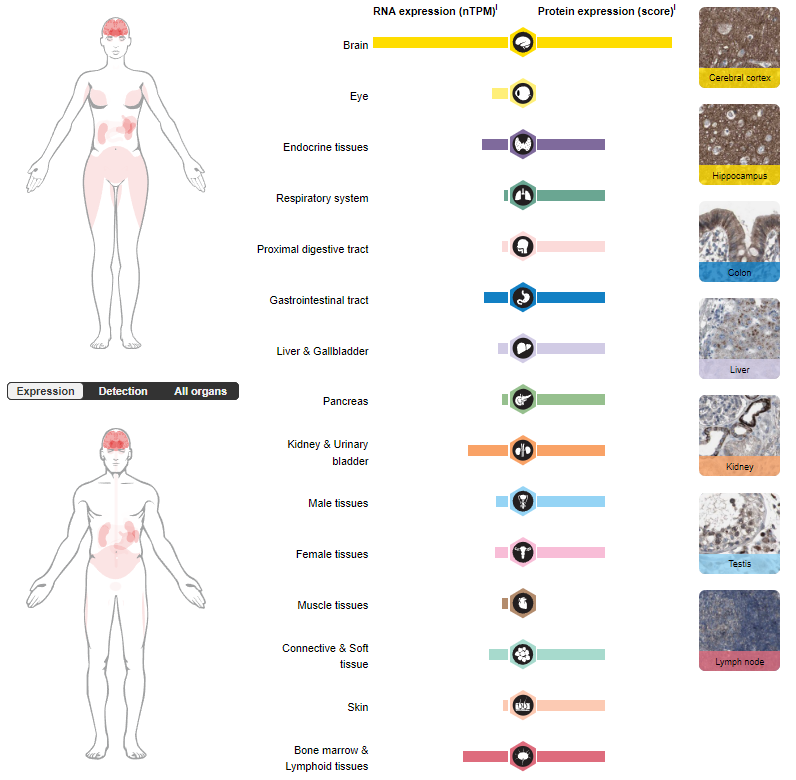
(数据来源 uniprot)
SSTR2的结构
SSTR2是一种七次跨膜蛋白,由369个氨基酸组成,其N端在胞外,C端在胞内。结构采用A类肽G蛋白偶联受体(GPCR)的典型活性态构象,包括类似的七跨膜螺旋(7TM)束,在细胞外环2(ECL2)形成的长的β-发夹结构和位于TM3和ECL2之间保守的二硫键。
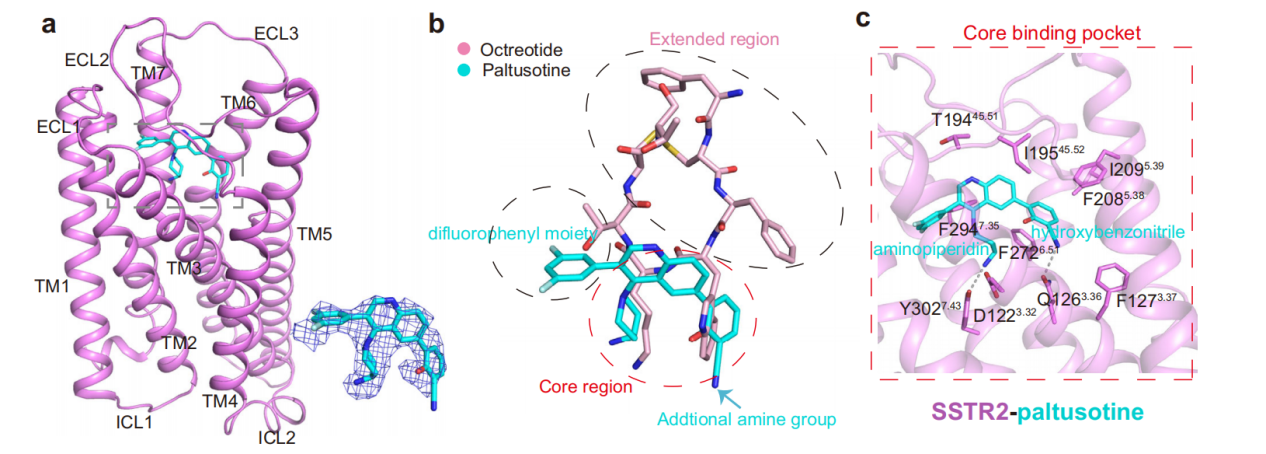
(数据来源 Zhao J, et al. Nat Commun. 2023)
SSTR2的信号转导
SSTR2或者其他生长抑素受体与SST结合后会发挥抗肿瘤作用,激活不同的磷酸酪氨酸磷酸酶(PTP)SHP-1和SHP-2以及PTPη。SHP-1通过激活转录因子NF-κB导致抑制MAP激酶JNK抗凋亡作用而引起细胞凋亡。SHP-2激活Src,Src直接与PTP η相互作用,诱导其酪氨酸磷酸化和激活。PTP η使参与细胞周期进程控制的细胞内效应器去磷酸化,例如ERK和PI3K/Akt通路,导致细胞周期蛋白激酶抑制剂p27,p21和肿瘤抑制基因Zac1上调。
SST与SSTR2结合后,SST通过抑制电压依赖性Ca 2+通道和激活K +通道来抑制多种激素的分泌/合成,从而减少细胞内Ca 2+浓度和抑制腺苷酸环化酶,降低细胞内cAMP水平。从而阻止癌基因的激活并抑制肿瘤的发生和进展。
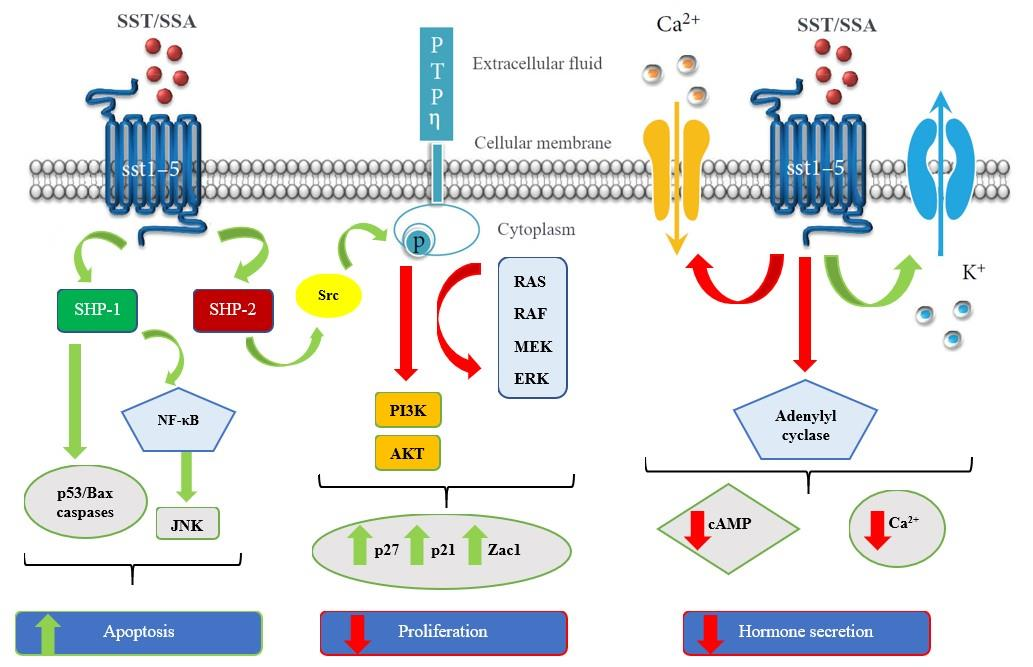
(数据来源 Eychenne R, et al. Molecules. 2020)
SSTR2的靶向治疗
目前靶向SSTR2的治疗方式主要是放射性核素疗法和合成多肽,靶向SSTR2的放射性核素疗法目前已经获批上市的是Lutetium Dotatate LU-177,除此之外还有大量放射性核素疗法在临床研究阶段。
[177Lu]Lu-DOTA-TATE于2017年获批上市,用于治疗神经内分泌瘤。治疗的分子基础是放射性标记的生长抑素类似物在表达SSTR-2的细胞的溶酶体中的内化和保留。在细胞内化后,β-辐射会导致细胞内DNA链的断裂和细胞死亡,并且还会产生低能伽马辐射,从而实现成像。因此,肿瘤及其转移灶均表达SSTR,并在生长抑素受体成像中显示出强烈的摄取,这对于治疗的功效至关重要。
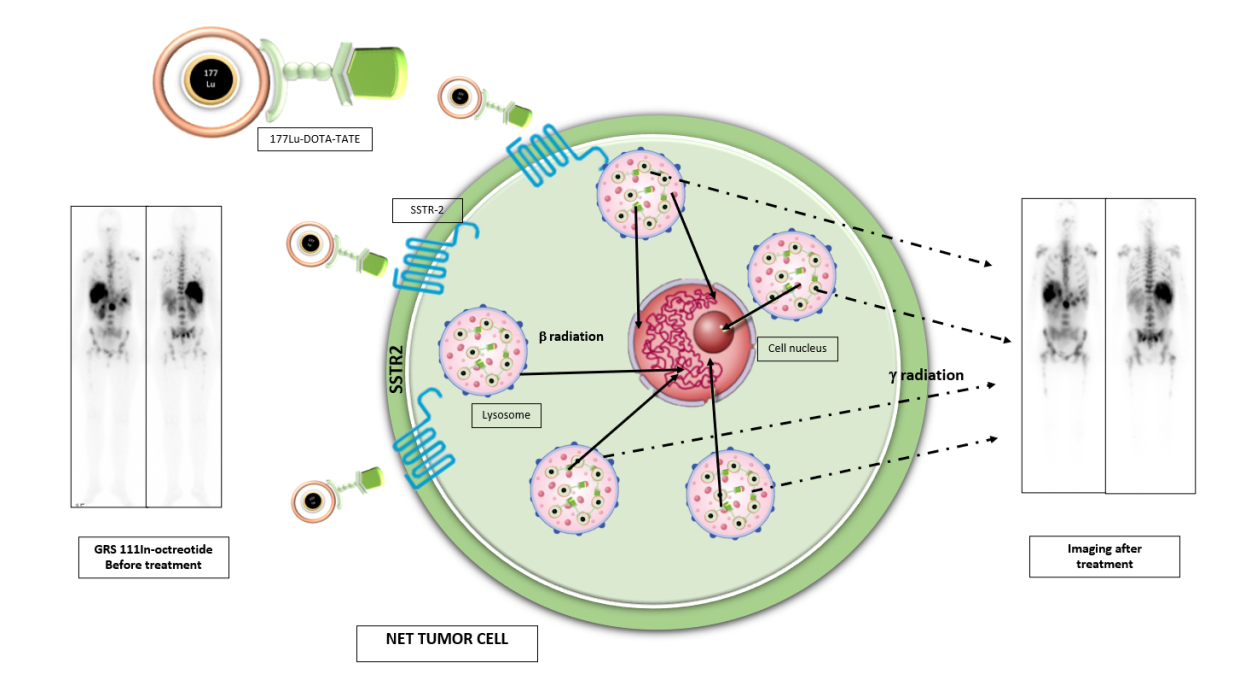
(数据来源 Del Olmo-Garcia MI, et al. Biomedicines. 2021)
CS-5005是一款靶向SSTR2的抗体药物偶联物,由基石药业开发,用于治疗实体瘤,目前还处于临床前研发阶段。基石药业还开发了一款靶向SSTR2的双特异性抗体CS-2012在临床前研究阶段,用于治疗实体瘤。
Tidutamab是由Xencor公司开发的靶向SSTR2/CD3的双特异性T细胞接合器,但是由于其疗效欠佳,目前已经终止其研发。
我们收集整理一批SSTR2相关抗体序列信息。文档可关注公众号,号内回复“SSTR2”下载。
