癌症是主要的公共卫生问题,是全球第二大死亡原因,其中乳腺癌和肺癌是最常见的两种癌症。由于激素疗法、化疗和放疗,乳腺癌生存率显著提高,但是乳腺癌的发病率仍然很高,乳腺癌仍然是女性癌症相关死亡的主要原因,这深刻反映了乳腺癌的异质性、转移和治疗耐药性。多年来,随着针对EGFR、ALK、ROS1和NTRK突变患者的酪氨酸激酶抑制剂的引入,肺癌的治疗也发生了变化,免疫检查点抑制剂(ICIs)也极大地改变了肺癌的治疗格局。尽管新的治疗方案在不断研发,但肺癌和乳腺癌的临床需求仍未得到满足,开发有前景的药理学策略以改善这两种癌症患者的临床结局至关重要。
2024年4月23日国家卫健委微生物药物生物技术重点实验室的研究人员在NPJ Precis Oncol上发表了一篇名为“A new TROP2-targeting antibody-drug conjugate shows potent antitumor efficacy in breast and lung cancers”的文章。本研究首先根据LDM分子特性,通过基因工程和分子重建相结合的方法制备了由抗体hIMB1636和分子LDM组成的新型ADC(hIMB1636- LDP - AE),并研究了其体内外抗乳腺癌和肺癌的活性。本研究充分证明了hIMB1636-LDP-AE对实体瘤的潜在作用,不仅为基于LDM的ADC提供了新的制备方法,而且为乳腺癌和肺癌的治疗提供了新的候选药物。

抗体-药物偶联物(ADC)概述
抗体偶联药物ADC被称为“生物导弹”,是一类新兴且发展迅速的靶向治疗药物,它是由一种肿瘤靶向抗体通过复杂设计的化学连接体与细胞毒性有效载荷偶联而成,使其能够同时选择性靶向和强毒性。2000年美国FDA首次批准的ADC药物Mylotarg®(gemtuzumab ozogamicin)用于急性髓系白血病(AML)成人患者,这标志着癌症靶向治疗的ADC时代的开始。到目前为止,全球已有15种ADC获得上市批准,用于血液系统恶性肿瘤和实体瘤的靶向治疗。
成功的ADC的关键要求包括选择合适的靶点、抗体、连接子和细胞毒性有效载荷,所有这些因素都会影响ADC的可给药特性,如抗肿瘤作用、药代动力学、稳定性和细胞毒性。虽然ADC的概念清晰明了,但要开发出抗体、连接子和有效载荷的合适组合的理想ADC仍然具有挑战性,因此,市售ADC仍然有限。选择合适的靶标是设计新型ADC的首要考虑因素。

(数据来源 Fu Z, et al. Signal Transduct Target Ther. 2022)
Trop2和LDM介绍
Trop2是滋养层细胞表面抗原2,又称肿瘤相关钙信号转导子2,是一种36kDa的细胞表面糖蛋白。Trop2在多种恶性肿瘤中表达上调,并参与导致肿瘤发生、侵袭和转移的几种致癌信号通路,但在正常人类组织中表达有限。因此,Trop2被认为是癌症治疗中一个有吸引力的治疗靶点。sacituzumab govitecan(SG;IMMU-132),含有人源化抗Trop -2单克隆抗体和拓扑异构酶抑制剂药物SN-38。它已被美国FDA批准用于治疗转移性三阴性乳腺癌患者。

(数据来源 Liu X, et al. Pharmacol Ther. 2022)
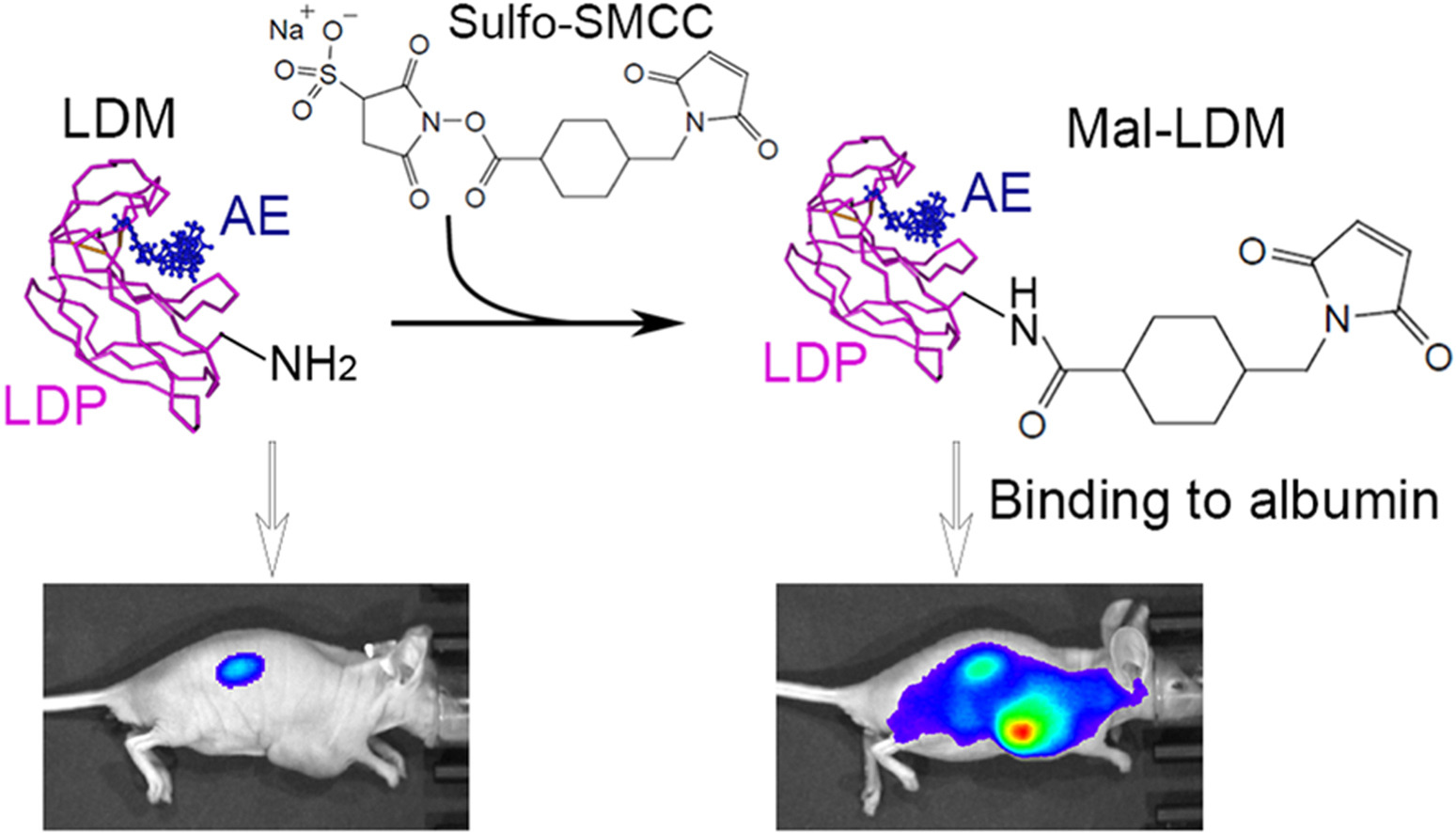
LDM是烯二炔类抗生素家族的一员,来源于球形链霉菌C1027,又称C-1027。在包括肝癌、乳腺癌、胰腺癌、结肠癌、肺癌、胃癌和脑癌在内的各种类型的癌症中,它显示出极强的细胞毒性和独特的抗肿瘤作用。LDM包含一个具有强大生物活性的烯二炔发色团(AE)和一个非共价结合的载脂蛋白(LDP),后者形成一个疏水口袋来保护发色团。AE和LDP可以自由分离和重组,重组后的LDM表现出与天然LDM相似的细胞毒性。
hIMB1636-LDP生成和鉴定
通过传统的杂交瘤技术和互补决定区(CDR)嫁接的人源化方法获得抗Trop2的人源化抗体hIMB1636,并发现在胰腺癌细胞来源的肿瘤模型中显示出良好的成像效果和显著的抗肿瘤效果,提示hIMB1636可作为肿瘤治疗的靶向载体。此外,hIMB1636可以被Trop2阳性的癌细胞内化并运输到溶酶体。

通过基因合成构建了hIMB1636- LDP蛋白的表达载体,经过转染、筛选、纯化后获得hIMB1636-LDP融合蛋白。SPR结果显示,hIMB1636-LDP对Trop2抗原具有很强的结合亲和力,表观平衡解离常数为4.57 nM;流式细胞术和免疫荧光分析,hIMB1636-LDP可在单细胞水平与Trop2高表达或中度表达的癌细胞结合。
hIMB1636-LDP功能鉴定
通过流式细胞术分析hIMB1636- LDP抗体和hIMB1636抗体对天然抗原的结合能力,发现LDP部分的连接不会对亲本抗体hIMB1636的结合活性产生不利影响。免疫荧光分析直接证实hIMB1636-LDP阳性被癌细胞内化进入靶细胞,且在小鼠异种移植模型中对肿瘤部位的荧光信号清晰可见,进一步证实了其在体内的肿瘤靶向性。

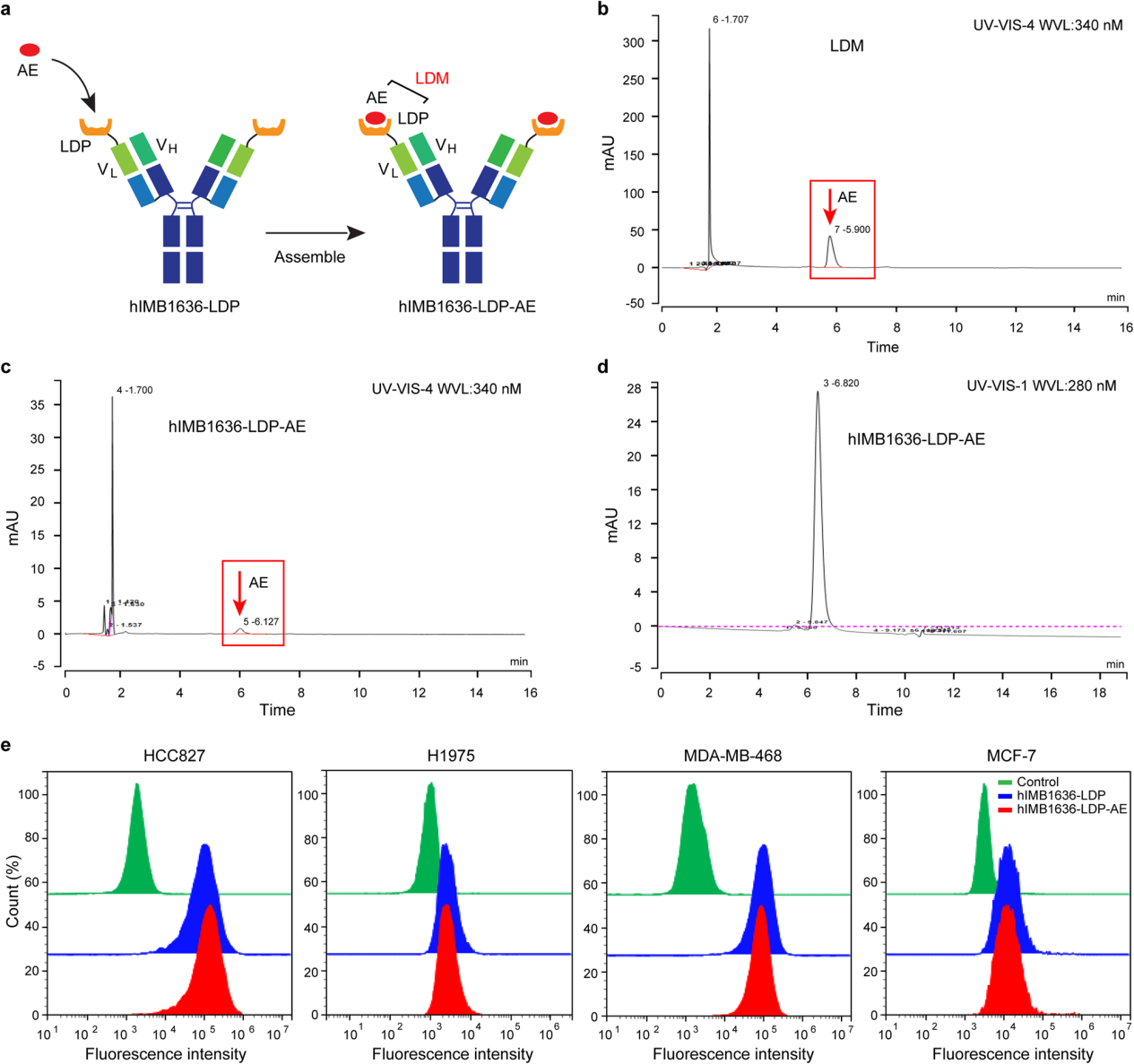
hIMB1636-LDP-AE组装
虽然hIMB1636-LDP对细胞表面Trop2抗原的强亲和力和特异性,但hIMB1636-LDP仍然需要一个有效载荷来直接执行细胞毒性,通过将烯二炔发色团AE组装到hIMB1636-LDP中,得到了含有两个LDM分子的融合蛋白hIMB1636-LDP-AE。流式细胞术分析组装过程几乎不影响抗体的亲和力,为其靶向能力的发挥提供了基础。
hIMB1636-LDP-AE抗肿瘤活性分析
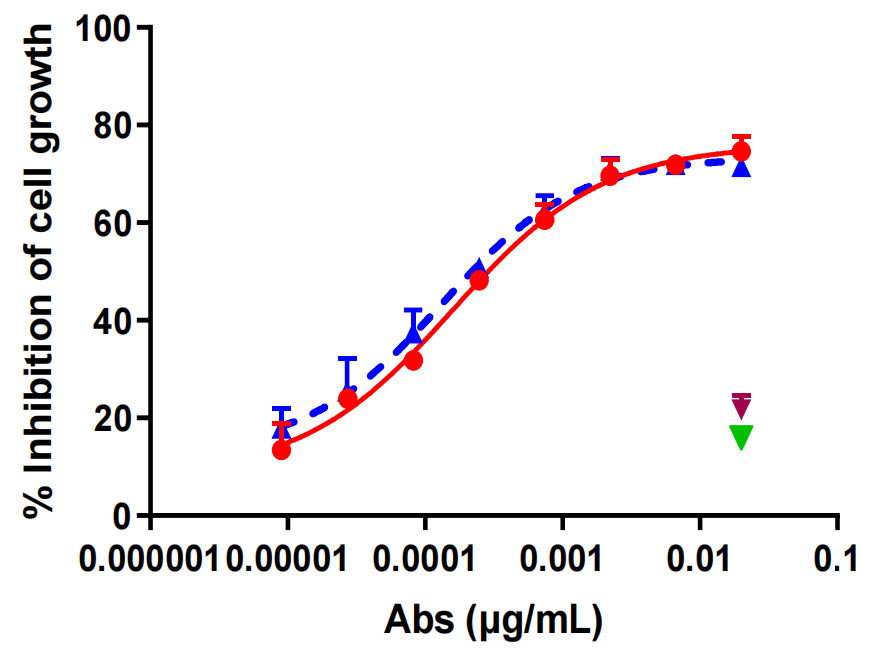
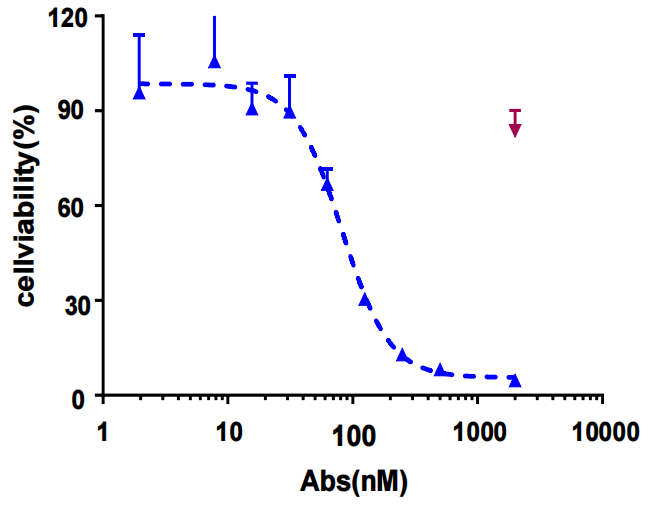
hIMB1636-LDP-AE在体外对Trop2阳性肿瘤细胞表现出显著的抗肿瘤活性,能够有效抑制肿瘤细胞的增殖和迁移,具有较高的细胞杀伤能力。

hIMB1636-LDP-AE体内抑制肿瘤生长
通过HCC827皮下异种移植模型,评估hIMB1636-LDP-AE在体内的抗肿瘤活性,发现hIMB1636-LDP-AE对HCC827异种移植物生长的抑制呈浓度依赖性。在HCC827和MDA-MB-468等Trop2阳性异种移植模型中,0.8 mg/kg的hIMB1636-LDP-AE治疗显著降低了肿瘤生长、肿瘤重量和肿瘤大小,具有较高的肿瘤抑制率。此外,在小鼠体内实验中,0.8 mg/kg的hIMB1636-LDP-AE治疗组未观察到明显的毒性病理变化,表明该剂量没有毒副作用。

分析hIMB1636-LDP-AE和SG在体内的抗肿瘤作用,结果表明,两者在HCC827(Trop2高表达)异种移植模型中均具有显著且明显相似的抗肿瘤作用。在MCF-7(Trop2中等表达)异种移植模型中,hIMB1636-LDP-AE表现出比SG更强的抑瘤效果,此外,hIMB1636-LDP-AE治疗未对血红蛋白、白细胞、血小板和中性粒细胞等血液参数产生明显影响,表明该ADC没有明显的骨髓毒性。

ADC纯度检测≥98%:
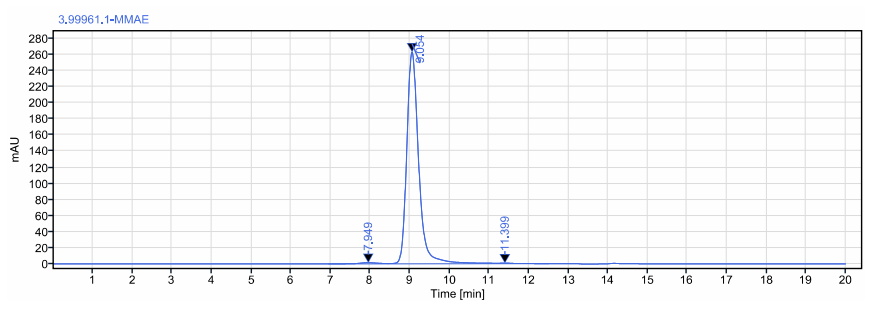
(SEC-HPLC)
ADC药物抗体比 (DAR) 检测3.7:
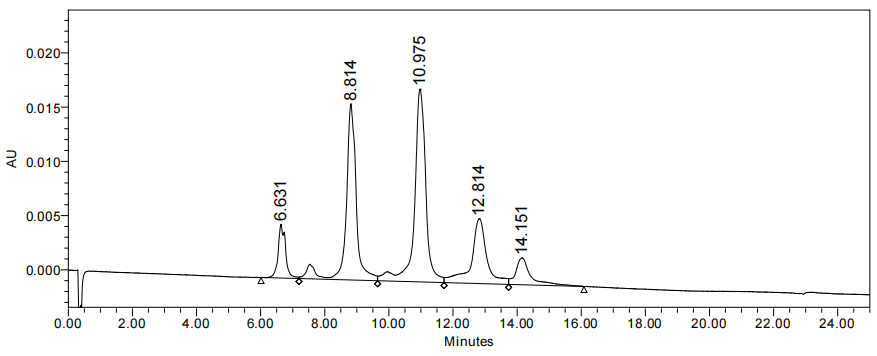
(HIC-HPLC)
ADC细胞内吞及毒性试验: